Questão 23668
UFU 2012
É bastante conhecido o efeito que a chuva ácida faz degradando esculturas de mármore. Porém outros materiais também sofrem degradação pela simples exposição à umidade, como é o caso das peças feitas de cobre, presentes nas cúpulas da Basílica de São Pedro, no Vaticano.
O cobre, quando em contato com o ar úmido e o gás carbônico, sofre um processo de oxidação formando carbonato de cobre II, que é o responsável pela coloração verde encontrada nas peças, conforme as equações (não-balanceadas).
A análise dessas equações químicas revela que
tanto o hidróxido de cobre II quanto o carbonato de cobre II são solúveis em água.
o cobre sofre processo de oxidação na primeira equação, variando seu Nox de zero para +2
em períodos chuvosos e poluídos em Roma, o efeito de corrosão da cúpula da Basílica de São Pedro é diminuído.
a primeira equação, quando balanceada, resulta, respectivamente, nos coeficientes 2, 2, 1, 2.
Gabarito:
o cobre sofre processo de oxidação na primeira equação, variando seu Nox de zero para +2
Resolução:
a) Os Hidróxidos e Carbonatos formados por metais de transição são praticamente insolúveis em água.
b) Conforme a equação abaixo o número de oxidação do cobre Cu varia de 0 para +2. Esse processo é denominado oxidação.
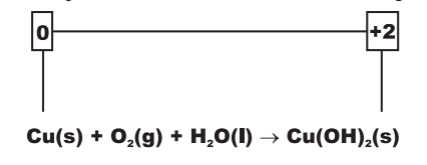
c) Em períodos chuvosos o ar se torna mais úmido favorecendo a transformação do cobre metálico em hidróxido de cobre II, substância de caráter básico. Em um período poluído a concentração de dióxido de carbono - substância de caráter ácido - presente na atmosfera aumenta, favorecendo a formação de carbonato de cobre dois, ao mentando assim a corrosão.
d) Primeira equação balanceada:
2 Cu(s) + 1 O2(g) + 2 H2O(l) 2 Cu(OH)2(s)