Questão 30050
UFSCAR 2009
(UFSCAR 2009)
Compostos orgânicos oxigenados como álcoois (ROH), cetonas (RCOR’), ésteres (RCOOR’) e ácidos carboxílicos (RCOOH’) são bastante presentes em nosso cotidiano. Por exemplo, etanol é usado como combustível para veículos, ácido acético é encontrado no vinagre, acetona e acetato de metila servem para remover esmalte de unhas. As propriedades de compostos dessas classes variam muito e a tabela ilustra alguns exemplos.
Assinale a alternativa que explica corretamente as propriedades descritas nessa tabela.
O ponto de ebulição do éster é menor que o ponto de ebulição da cetona, porque o maior número de átomos de oxigênio presente na molécula do éster aumenta as interações dipolo-dipolo, que desfavorecem as interações entre suas moléculas.
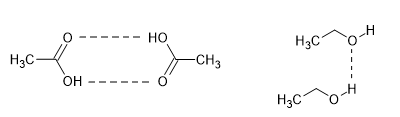
O ácido carboxílico é um composto polar e faz fortes ligações hidrogênio entre suas moléculas, o que explica o elevado ponto de ebulição.
O éster é mais polar que o ácido, por isso há mais interações dipolo induzido entre suas moléculas, o que explica o ponto de ebulição mais baixo observado para o éster.
A cetona tem massa molecular menor que o ácido, por isso seu ponto de ebulição é menor.
O álcool tem o menor ponto de fusão dentre os compostos listados, porque pode formar o maior número de ligações hidrogênio, devido ao maior número de átomos de hidrogênio presente em sua molécula.
Gabarito:
O ácido carboxílico é um composto polar e faz fortes ligações hidrogênio entre suas moléculas, o que explica o elevado ponto de ebulição.
Resolução:
a) O ponto de ebulição do éster é menor que o ponto de ebulição da cetona, porque o maior número de átomos de oxigênio presente na molécula do éster aumenta as interações dipolo-dipolo, que desfavorecem as interações entre suas moléculas.
Incorreta. O maior número de átomos de oxigênio no estér diminui as interações dipolo-dipolo, que desfavorecem as interações entre as suas moléculas, resultando num ponto de ebulição menor.
b) Correta. O ácido carboxílico é um composto polar e faz fortes ligações hidrogênio entre suas moléculas, o que explica o elevado ponto de ebulição.
c) O éster é mais polar que o ácido, por isso há mais interações dipolo induzido entre suas moléculas, o que explica o ponto de ebulição mais baixo observado para o éster.
Incorreta. A justificativa correta para as diferenças das temperaturas de ebulição desses dois compostos é a diferença nas interações intermoleculares. As interações intermoleculares do ácido são ligações de hidrogênio e as do éster dipolo-dipolo. Como as ligações de hidrogênio são interações mais fortes do que as dipolo-dipolo, o ácido apresenta maior temperatura de ebulição.
d) A cetona tem massa molecular menor que o ácido, por isso seu ponto de ebulição é menor.
Incorreta. A justificativa correta para as diferenças das temperaturas de ebulição desses dois compostos é a diferença nas interações intermoleculares. As interações intermoleculares do ácido são ligações de hidrogênio e as da cetona dipolo-dipolo. Como as ligações de hidrogênio são interações mais fortes do que as dipolo-dipolo, o ácido apresenta maior temperatura de ebulição.
e) O álcool tem o menor ponto de fusão dentre os compostos listados, porque pode formar o maior número de ligações hidrogênio, devido ao maior número de átomos de hidrogênio presente em sua molécula.
Incorreta. Dos compostos listados, somente o álcool e o ácido carboxílico fazem ligações de hidrogênio. O que faz o maior número de ligações de hidrogênio é o ácido.