Questão 65126
UFSCAR 2005
(UFSCAR 2005)
A dissolução de uma substância em água pode ocorrer com absorção ou liberação de calor. O esquema apresenta as temperaturas da água destilada e das soluções logo após as dissoluções do nitrato de sódio e hidróxido de cálcio em água destilada.
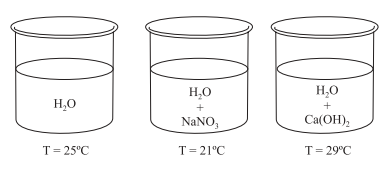
Os gráficos seguintes representam as curvas de solubilidade para as duas substâncias consideradas.
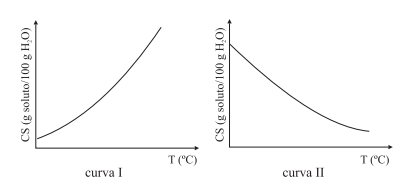
Quanto ao calor liberado ou absorvido na dissolução, o calor de dissolução (∆Hdiss) e a curva de solubilidade, assinale a alternativa que apresenta as propriedades que correspondem, respectivamente, à dissolução do nitrato de sódio e à do hidróxido de cálcio em água.
Endotérmica; ∆Hdiss > 0; curva I.
Exotérmica; ∆Hdiss < 0; curva II.
Endotérmica; ∆Hdiss > 0; curva II.
Exotérmica; ∆Hdiss < 0; curva I.
Exotérmica; ∆Hdiss > 0; curva I.
Endotérmica; ∆Hdiss < 0; curva II.
Exotérmica; ∆Hdiss < 0; curva I.
Endotérmica; ∆Hdiss > 0; curva II.
Exotérmica; ∆Hdiss > 0; curva II.
Endotérmica; ∆Hdiss < 0; curva I.
Gabarito:
Endotérmica; ∆Hdiss > 0; curva I.
Exotérmica; ∆Hdiss < 0; curva II.
Resolução:
A dissolução do NaNO3 é endotérmica, pois houve diminuição da temperatura da água, o que significa que o NaNO3 absorveu calor da água. Com isso ∆H > 0.
Já a dissolução do Ca(OH)2 é exotérmica, por ter aumento da temperatura da água, como mostra o gráfico, indicando que a dissolução cedeu calor para a água, e portanto, ∆H < 0.