Questão 10112
UFRGS 2013
(UFRGS - 2013)
Os potenciais padrão de redução, determinados mediante processos eletroquímicos, podem ser empregados para prever a espontaneidade de reações, mesmo quando essas não constituem pilhas ou baterias.
Observe o quadro a seguir.
Com base no quadro, considere as reações abaixo.
Quais reações serão espontâneas?
Apenas I.
Apenas II.
Apenas III.
Apenas I e III.
I, II e III.
Gabarito:
Apenas III.
Resolução:
Para que uma reação seja espontânea, o seu valor de ΔE > 0.
Por isso, é preciso calcular o valor de ΔE de cada uma das reações.
I) Ba(NO3)2 + 2Ag → 2AgNO3 + Ba
Nessa reação, a variação de NOx é:
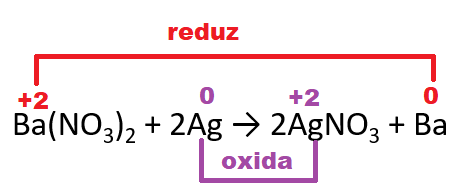
O potencial pode ser calculado com várias fórmulas:
ΔE = Eo(oxi. maior) - Eo(oxi. menor)
ΔE = Eo(red. maior) - Eo(red. menor)
ΔE = Eo(red) + Eo(oxi)
Nessa resolução será utilizado: ΔE = Eo(red) + Eo(oxi)
O potencial da reação Ba(NO3)2 + 2Ag → 2AgNO3 + Ba vai ser.
ΔE = Eo(red) + Eo(oxi)
ΔE = -2,90 + (- 0,80)
ΔE = - 3,70V
Como ΔE < 0, é não espontânea.
II) 2Al(NO3)3 + 3CO → 3CO(NO3)2 + 2Al
Nessa reação, a variação de NOx é:
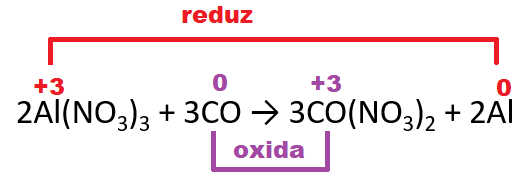
O potencial da reação 2Al(NO3)3 + 3CO → 3CO(NO3)2 + 2Al vai ser.
ΔE = Eo(red) + Eo(oxi)
ΔE = -1,66 + 0,28
ΔE = - 1,34V
Como ΔE < 0, é não espontânea.
III) 3AgNO3 + 3Al → Al(NO3)3 + 3Ag
Nessa reação, a variação de NOx é:
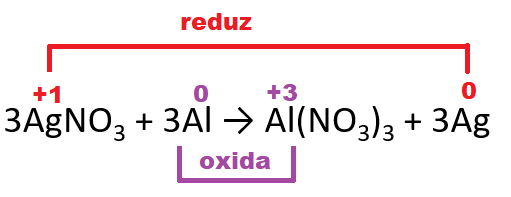
O potencial da reação 3AgNO3 + 3Al → Al(NO3)3 + 3Ag vai ser.
ΔE = Eo(red) + Eo(oxi)
ΔE =+0,80 + 1,66
ΔE = +2,46V
Como ΔE > 0, é espontânea.