Questão 69214
UFRGS 2012
(UFRGS - 2012)
A coluna da esquerda, abaixo, apresenta cinco espécies moleculares que têm o elemento enxofre como átomo central, a da direita, tipos, de geometria molecular que correspondem a quatro dessas espécies. Associe corretamente a coluna da direita à da esquerda.
|
1. SO2 2. SOCl2 3. H2SO4 4. SO3 5. H2S |
( ) trigonal plana ( ) tetraédrica ( ) piramidal ( ) angular |
A sequência correta de preenchimento dos parênteses, de cima para baixo, é:
2 - 3 - 1 - 4.
2 - 4 - 3 - 1.
3 - 2 - 1 - 5.
4 - 3 - 2 - 1.
4 - 2 - 3 - 5.
Gabarito:
4 - 3 - 2 - 1.
Resolução:
Analisando a geometria de todos os compostos:
1. SO2
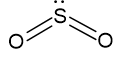
Pela presença de par de elétrons livres, o SO2 terá geometria angular.
2. SOCl2
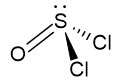
Pela presença de par de elétrons livres e 3 ligantes, esse é um composto de geometria piramidal.
3. H2SO4
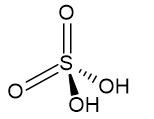
Por apresentar 4 ligantes e não ter elétrons livres, o H2SO4 terá geometria tetraédrica.
4. SO3
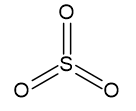
Por apresentar 3 ligantes e nenhum par de elétron livre, terá geometria trigonal plana.
5. H2S
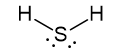
Pela presença de pares de elétrons livres e 2 ligantes, terá geometria angular.