Questão 18
UFPR 2018
(UFPR - 2018 - 1ª FASE)
Erupções vulcânicas e queima de combustíveis fósseis são fontes de emissão de dióxido de enxofre para a atmosfera, sendo este gás responsável pela chuva ácida. Em laboratório, pode-se produzir o SO2 (g) em pequena escala a partir da reação entre cobre metálico e ácido sulfúrico concentrado. Para evitar o escape desse gás para a atmosfera e que seja inalado, é possível montar uma aparelhagem em que o SO2 (g) seja canalizado e borbulhado numa solução salina neutralizante.
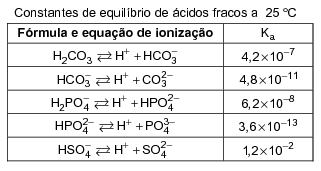
Com base nas informações fornecidas, qual dos sais indicados a seguir é o mais eficiente como solução neutralizante?
Sulfato de sódio.
Carbonato de sódio.
Fosfato de sódio.
Hidrogenocarbonato de sódio.
Monohidrogenofosfato de sódio.
Gabarito:
Fosfato de sódio.
Resolução:
A questão pede uma "solução salina neutralizante", dessa forma precisamos de uma solução que seja a mais básica.
Através dos valores de Ka conseguimos definir os ácidos fortes e fracos dispostos na tabela, como precisamos de uma solução básica, e quanto mais fraco é o ácido, mais forte é sua base conjugada, vamos utilizar o ácido com o menor valor de Ka (quanto menor o Ka, mais fraco é o ácido).
HPO42- ⇌ H+ + PO43-