Questão 68477
UFJF 2019
(UFJF - 2019)
O nitrato de potássio é um composto químico sólido, bastante solúvel em água, muito utilizado em explosivos, estando presente na composição da pólvora, por exemplo. Uma equação termoquímica balanceada para a queima da pólvora é representada abaixo:
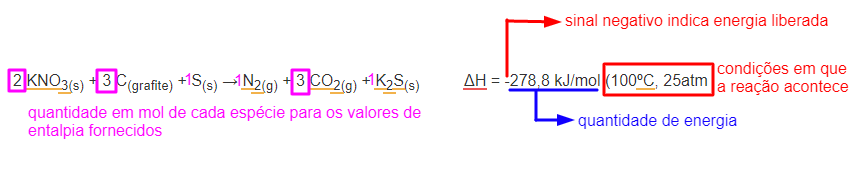
| 2 KNO3(s) + 3 C(grafite) + S(s) → N2(g) + 3 CO2(g) + K2S(s) | ΔH = -278,8 kJ/mol (100ºC, 25atm) |
Assinale a alternativa que representa a interpretação correta da equação termoquímica para a queima da pólvora:
Durante a queima da pólvora ocorre a absorção de 278,8kJ/mol de energia, o que acarreta um aumento da temperatura em 100ºC e o aumento da pressão em 25 atmosferas.
Durante a queima da pólvora ocorre a liberação de 278,8kJ/mol de energia, o que acarreta um aumento da temperatura em 100ºC e o aumento da pressão em 25 atmosferas.
Durante a queima da pólvora ocorre a liberação de 278,8kJ/mol de energia, levando ao aumento da temperatura para 100ºC e ao aumento da pressão para 25 atmosferas.
Durante a queima da pólvora ocorre a absorção de 278,8 kJ/mol de energia, se a reação for feita em 100ºC e 25 atmosferas.
Durante a queima da pólvora ocorre a liberação de 278,8 kJ/mol de energia, se a reação for feita em 100ºC e 25 atmosferas.
Gabarito:
Durante a queima da pólvora ocorre a liberação de 278,8 kJ/mol de energia, se a reação for feita em 100ºC e 25 atmosferas.
Resolução:
a) Incorreto. Durante a queima da pólvora ocorre a absorção de 278,8kJ/mol de energia, o que acarreta um aumento da temperatura em 100ºC e o aumento da pressão em 25 atmosferas.
100ºC e 25atm são as condições de temperatura e pressão na qual a reação ocorre liberando 278,8 kJ de energia
b) Incorreto. Durante a queima da pólvora ocorre a liberação de 278,8kJ/mol de energia, o que acarreta um aumento da temperatura em 100ºC e o aumento da pressão em 25 atmosferas.
100ºC e 25atm são as condições de temperatura e pressão na qual a reação ocorre liberando 278,8 kJ de energia
c) Incorreto. Durante a queima da pólvora ocorre a liberação de 278,8kJ/mol de energia, levando ao aumento da temperatura para 100ºC e ao aumento da pressão para 25 atmosferas.
100ºC e 25atm são as condições de temperatura e pressão na qual a reação ocorre liberando 278,8 kJ de energia
d) Incorreto. Durante a queima da pólvora ocorre a absorção de 278,8 kJ/mol de energia, se a reação for feita em 100ºC e 25 atmosferas.
Ocorre a liberação, pois o sinal de ΔH é negativo, indicando uma reação exotérmica.
e) Correto. Durante a queima da pólvora ocorre a liberação de 278,8 kJ/mol de energia, se a reação for feita em 100ºC e 25 atmosferas