Questão 64777
UDESC 2014
(UDESC 2014)
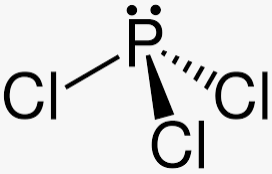
O tricloreto de fósforo (PCl3) é um líquido incolor bastante tóxico com larga aplicação industrial, principalmente na fabricação de defensivos agrícolas. A respeito deste composto é correto afirmar que:
a molécula é polar, pois o momento de dipolo resultante não é nulo.
as ligações entre os átomos de cloro e o átomo de fósforo são iônicas devido à elevada diferença de eletronegatividade entre estes não-metais.
a geometria molecular deste composto é trigonal plana, uma vez que esta estrutura apresenta menor energia (menor repulsão eletrônica).
após a formação da molécula o átomo central de fósforo efetua ligações do tipo π.
ao entrar em contato com água o PCl3 reage violentamente, gerando HCl, tornando o meio reacional básico.
Gabarito:
a molécula é polar, pois o momento de dipolo resultante não é nulo.
Resolução:
a) Correto. a molécula é polar, pois o momento de dipolo resultante não é nulo.
b) Incorreto. as ligações entre os átomos de cloro e o átomo de fósforo são iônicas devido à elevada diferença de eletronegatividade entre estes não-metais.
A diferença de eletronegatividade entre o cloro (3,1) e o fósforo (2,1) é menor que 1,7 e portanto não configura ligação iônica, além disso, por convenção, ligações entre ametais são covalentes
c) Incorreto. a geometria molecular deste composto é trigonal plana, uma vez que esta estrutura apresenta menor energia (menor repulsão eletrônica).
a geometria é piramidal, devido à presença de par de elétrons livres no composto
d) Incorreto. após a formação da molécula o átomo central de fósforo efetua ligações do tipo π.
há apenas ligações sigma
e) Incorreto. ao entrar em contato com água o PCl3 reage violentamente, gerando HCl, tornando o meio reacional básico.
Gera sim, HCl, porém o meio reacional é ácido