Questão 54417
UDESC 2012
(UDESC - 2012)
O último elétron de um átomo neutro apresenta o seguinte conjunto de números quânticos: n = 3; l= 1; m = 0; s = +1/2. Convencionando-se que o primeiro elétron a ocupar um orbital possui número quântico de spin igual a +1/2, o número atômico desse átomo é igual a:
15
14
13
17
16
Gabarito:
14
Resolução:
O último elétron do átomo possui os números quânticos n = 3; l= 1; m = 0; s = +1/2. O número quântico secundário l = 1 é referente ao orbital p. O número quântico magnético m = 0 é referente ao segundo orbital p. Como a convenção é de que o primeiro elétron a ocupar um orbital tem número quântico de spin +1/2, esse elétron é o primeiro a ocupar o segundo orbital 3p. Utilizando o diagrama de caixas para representar os orbitais, esse orbital seria o que está marcado de azul na imagem abaixo:
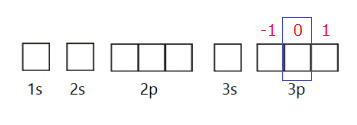
Fazendo a distribuição eletrônica de um átomo seguindo o diagrama de Pauling, todos os orbitais antes do 3p devem ser ocupados antes de preenchermos esse orbital. Em seguida, preenchemos os orbitais p com um elétron cada para depois emparelhar os elétrons. Então a distribuição eletrônica seria assim:
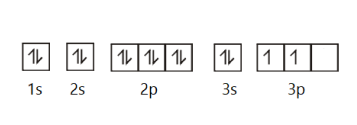
Ou 1s2 2s2 2p6 3s2 3p2. O número de elétrons dessa distribuição eletrônica é 14. Essa espécie ser um átomo significa que ela é eletricamente neutra, ou seja, o número de prótons é igual ao número de elétrons. O número atômico de um átomo é igual ao número de prótons, então o número atômico desse átomo é 14.