Questão 68505
MACKENZIE 2013
Química
(Mackenzie - 2013)
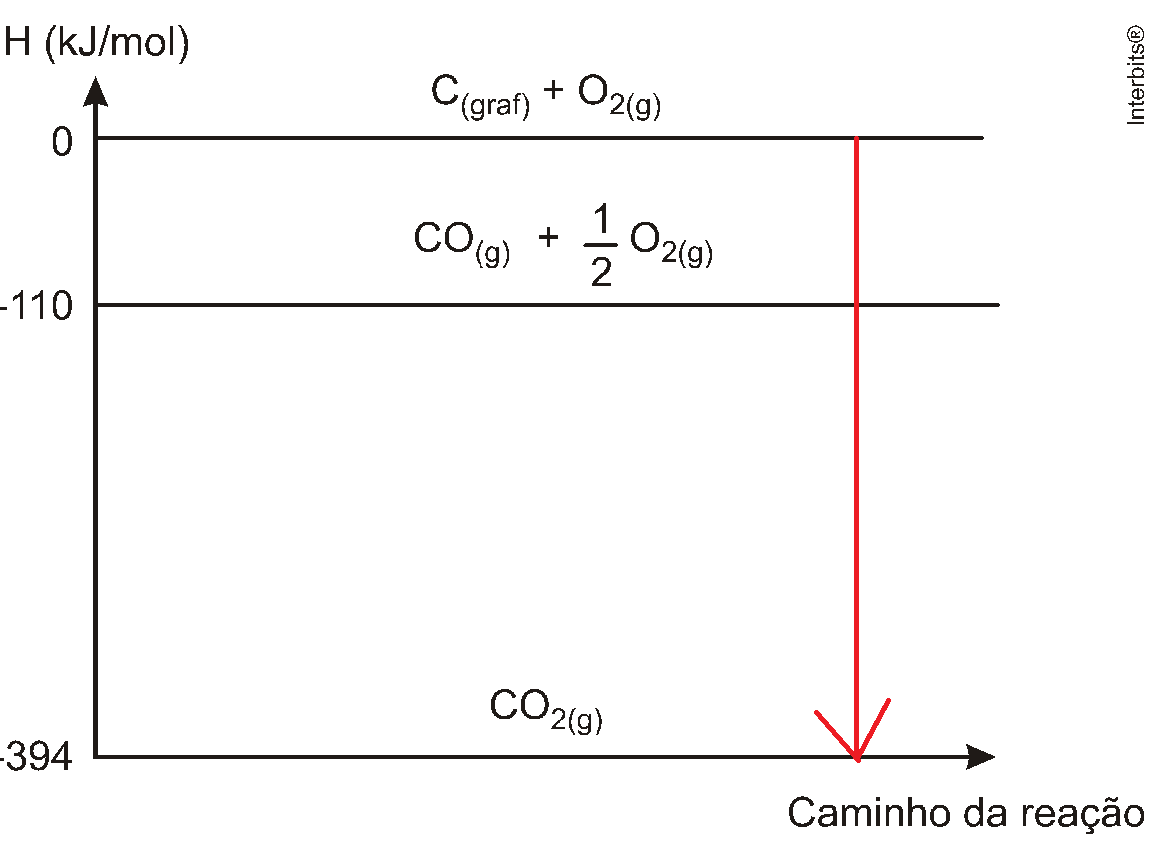
Observe o gráfico de entalpia abaixo, obtido por meio de experimentos realizados no estado-padrão:
Com base em seus conhecimentos de termoquímica e nas informações do gráfico acima, a equação termoquímica INCORRETAMENTE representada é
A
| CO2(g) → C(graf) + O2(g) | ΔHº = +394 kJ/mol |
B
| CO(g) + 1/2 O2(g) → CO2(g) | ΔHº = -284 kJ/mol |
C
| C(graf) + 1/2 O2(g) → CO(g) | ΔHº = +110 kJ/mol |
D
| CO2(g) → CO(g) + 1/2 O2(g) | ΔHº = +284 kJ/mol |
E
| C(graf) + O2(g) → CO2(g) | ΔHº = -394 kJ/mol |
Gabarito:
| C(graf) + 1/2 O2(g) → CO(g) | ΔHº = +110 kJ/mol |
Resolução:
a) Correto.
| CO2(g) → C(graf) + O2(g) | ΔHº = +394 kJ/mol |
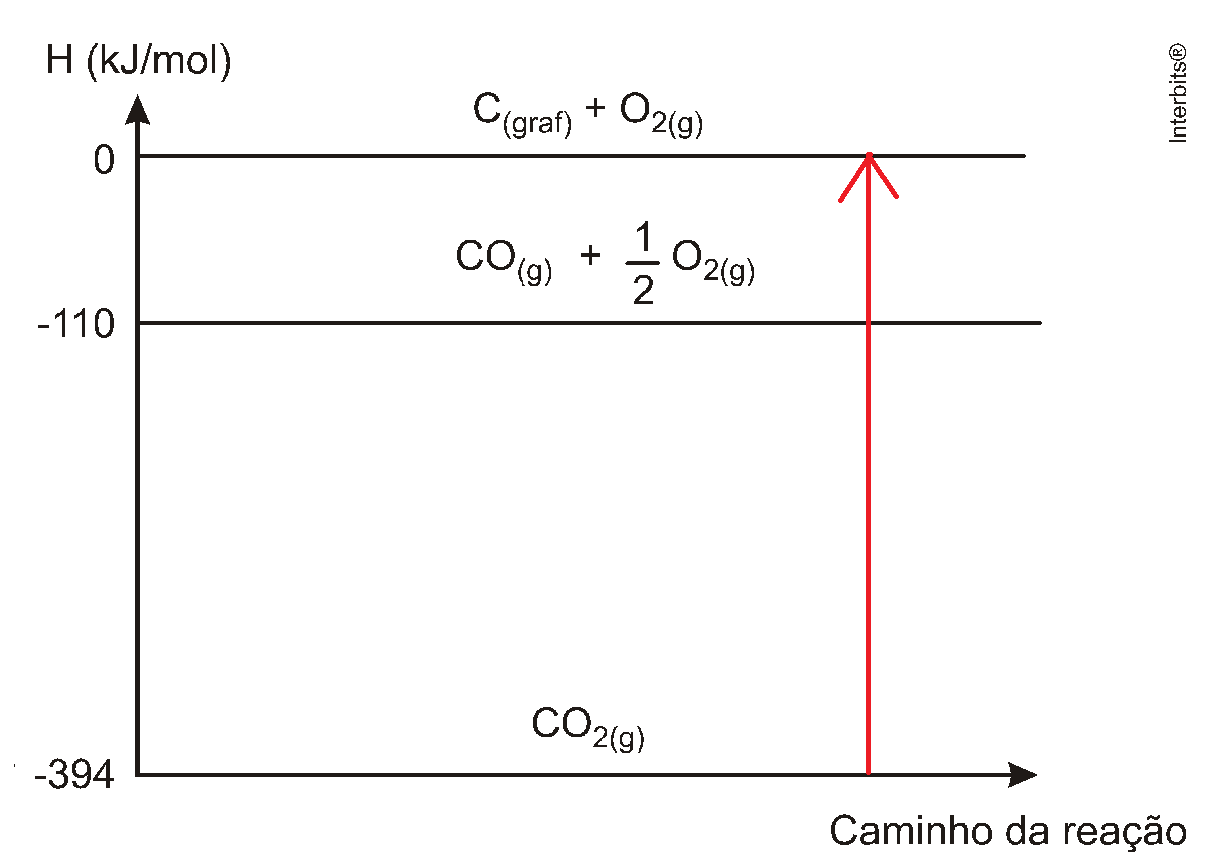
ΔH = Hprodutos -Hreagentes
ΔH = 0 - (-394) = +394
b) Correto.
| CO(g) + 1/2 O2(g) → CO2(g) | ΔHº = -284 kJ/mol |
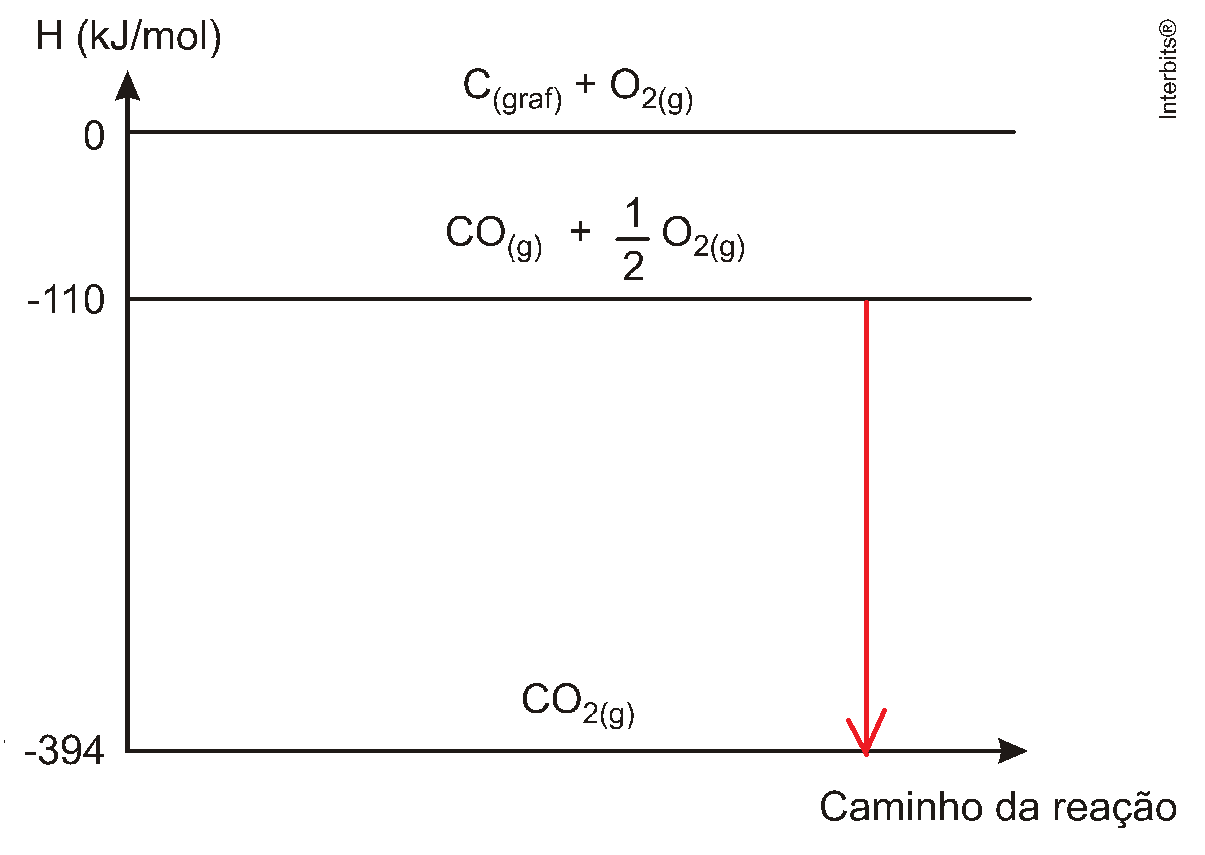
ΔH = Hprodutos -Hreagentes
ΔH = -394 - (-110) = -284
c) Incorreto.
| C(graf) + 1/2 O2(g) → CO(g) | ΔHº = +110 kJ/mol |
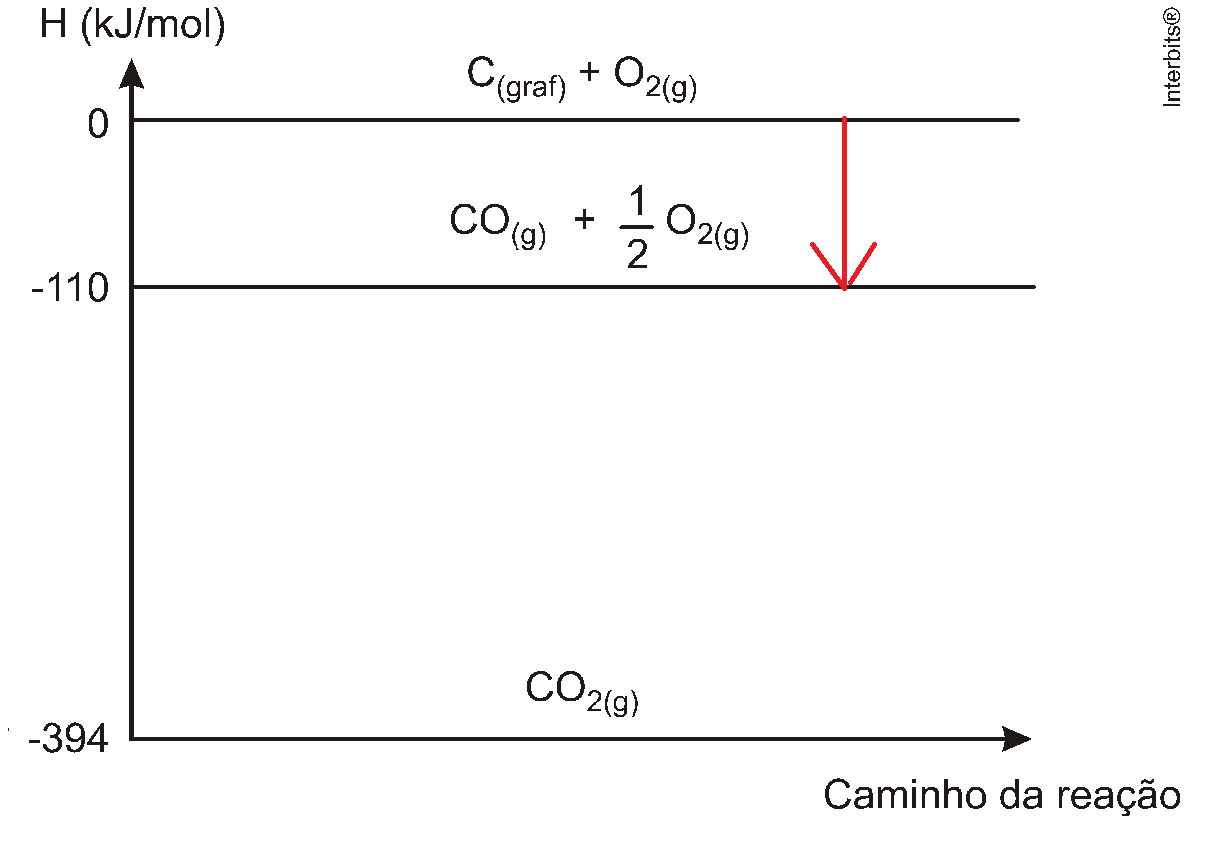
ΔH = Hprodutos -Hreagentes
ΔH = -110 - 0 = -110
d) Correto.
| CO2(g) → CO(g) + 1/2 O2(g) | ΔHº = +284 kJ/mol |
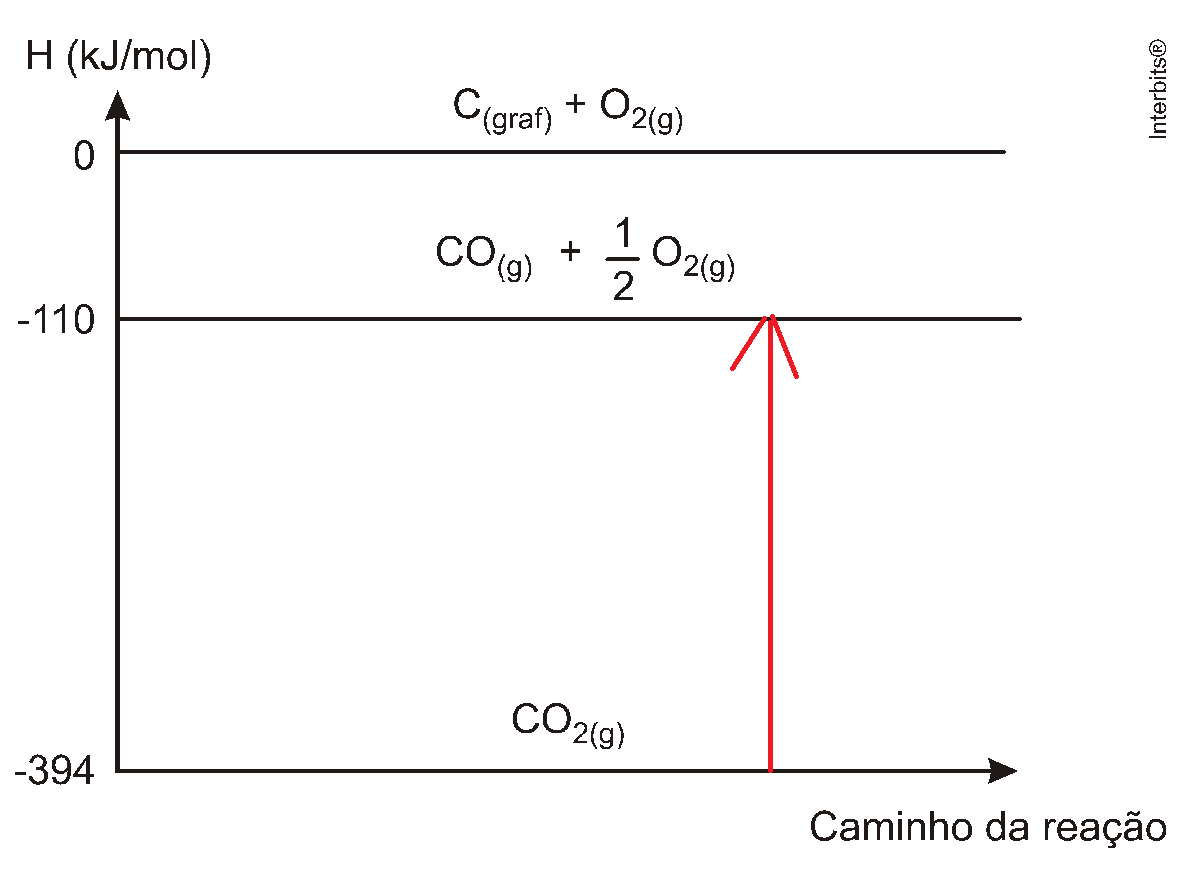
ΔH = Hprodutos -Hreagentes
ΔH = -110 - (-394) = +284
e) Correto.
| C(graf) + O2(g) → CO2(g) | ΔHº = -394 kJ/mol |
ΔH = Hprodutos -Hreagentes
ΔH = -394 - 0 = -394