Questão 58
ITA 2019
(ITA - 2019 - 1ª FASE)
A reação de adição nucleofílica de dienos conjugados pode levar à formação de produtos 1,2-substituídos ou 1,4-substituídos, dependendo das condições de temperatura e de estrutura do reagente.
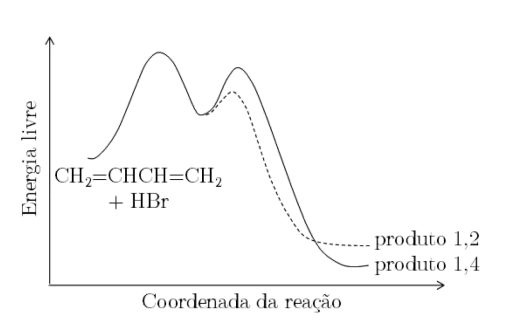
A figura mostra o diagrama de energia em função da coordenada de reação para a adição de HBr a 1,3-butadieno. Com base nessa figura, sejam feitas as seguintes afirmações:
I. O produto 1,2 deve se formar mais rapidamente que o produto 1,4.
II. O produto 1,4 é termodinamicamente mais estável que o produto 1,2.
III. Independentemente da temperatura de reação, há a formação de um intermediário comum a partir do qual os produtos são formados.
IV. Se a temperatura for suficiente para fornecer energia aos reagentes e intermediários para formar os produtos, mas não for suficiente para reverter produtos em intermediários, o produto 1,2 será formado majoritariamente.
Das afirmações acima, está(ão) CORRETA(S)
apenas I e II
apenas I e IV
apenas II, III e IV
apenas III
todas
Gabarito:
todas
Resolução:
I. Correta. Na 2ª etapa da reação, a energia de ativação da reação que forma o produto 1,2 é menor do que a do produto 1,4, e assim deve ser mais rápida.
II. Correta. Como a Energia Livre de Gibbs do produto 1,4 é menor que a do produto 1,2, o produto 1,4 é termodinamicamente mais estável.
III. Correta. A primeira etapa da reação é idêntica para as duas reações e forma um mesmo intermediário. De fato, o mecanismo que ocorre nas duas etapas é:
H2C = CH - CH = CH2 + HBr → H2C = CH - CH - CH3 + Carbocátion secundário (mais estável)
IV. Correta. Como na 2ª etapa da reação a energia de ativação para a obtenção do produto 1,2 é menor, para uma menor energia de ativação na reação inversa, o produto 1,2 deve reagir mais facilmente. Assim, o produto 1,2 será obtido majoritariamente.