Questão 4
ITA 2016
(ITA - 2016 - 1ª Fase)
A respeito de reações químicas descritas pela equação de Arrhenius, são feitas as seguintes proposições:
I. Para reações bimoleculares, o fator pré-exponencial na equação de Arrhenius é proporcional à frequência de colisões, efetivas ou não, entre as moléculas dos reagentes.
II. O fator exponencial na equação de Arrhenius é proporcional ao número de moléculas cuja energia cinética relativa é maior ou igual à energia de ativação da reação.
III. Multiplicando-se o negativo da constante dos gases (−R) pelo coeficiente angular da reta ln k versus 1/T obtém-se o valor da energia de ativação da reação.
IV. O fator pré-exponencial da equação de Arrhenius é determinado pela intersecção da reta ln k versus 1/T com o eixo das abscissas.
Das proposições acima, esta(ao) ERRADA(S)
apenas I.
apenas I e II.
apenas I e IV.
apenas II e III.
apenas IV.
Gabarito:
apenas IV.
Resolução:
I. CORRETA. Com a geometria correta, o fator pré-exponencial A está relacionado com a frequência de colisões, efetivas ou não.
ou
II. CORRETA. O fator exponencial na equação de Arhennius é a fração de moléculas reagente, ou seja, com energia suficiente para reagir. Essa energia cinética relativa é igual ou maior do que a energia de ativação da reação.
III. CORRETA.
É uma equação de primeiro grau, onde é a função que se pode expressar num gráfico de
.
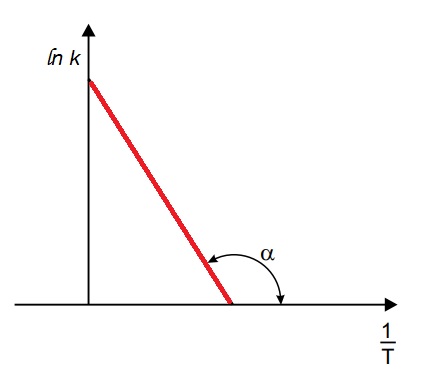
O coeficiente angular:
IV) INCORRETA.
Se tende a 0, portanto
. Assim, o valor do logaritmo neperiano do pré-fator A é detemrinado pela intersecção da reta com o eixo das ordenadas
e não o fator pré-exponencial da Equação de Arrhenius.
Gabarito E.