Questão 8
ITA 2013
(ITA 2013 - 2 fase)
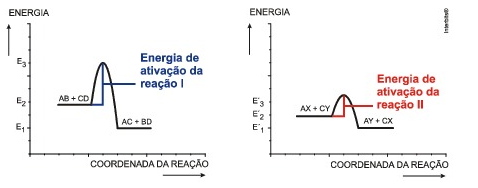
Os diagramas seguintes, traçados numa mesma escala, referem-se, respectivamente, aos equilíbrios, em fase gasosa e numa mesma temperatura, representados pelas seguintes equações químicas:
Comparando as informações apresentadas nos dois diagramas, pedem-se:
a) Qual das constantes de equilíbrio, K1 ou K2 terá valor maior? Justifique sua resposta.
Dado eventualmente necessário: A relação entre a variação da Energia Livre de Gibbs padrão ΔG0 e a constante de equilíbrio (K) de uma reação é dada por ΔG0= - RT·lnk.
b) Para as seguintes misturas numa mesma temperatura:
Qual das reações químicas, expressa pela equação I ou II, atinge o equilíbrio mais rapidamente? Justifique sua resposta.
Gabarito:
Resolução:
a) A variação da energia de gibbs é calculada por:
Para as duas reações, a energia de Gibbs será:
A partir dos diagramas:
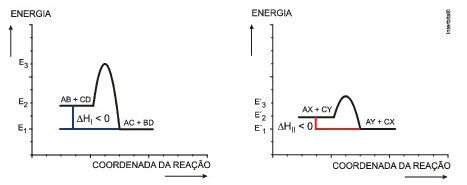
• |ΔHI| > |ΔHII|
• |ΔGI| > |ΔGII|
A constante de equilíbrio de uma reação é dada por , então:
Como:
b) Analisando o gráfico, a energia de ativação da reação I é maior que a da II: