Questão 8
ITA 2012
(ITA - 2012 - 2ª Fase)
A figura apresenta o diagrama de distribuição de espécies para o ácido fosfórico em função do pH.
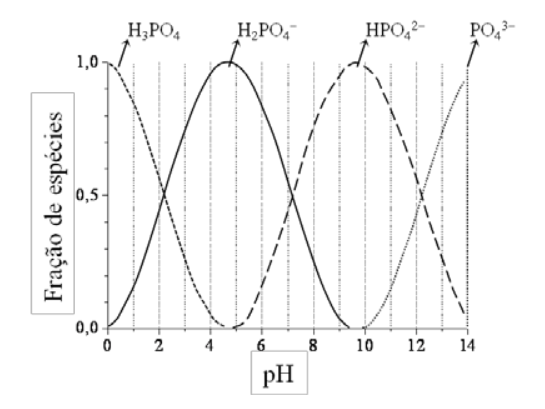
Com base nesta figura, pedem-se:
a) Os valores de pKa1, pKa2 e pKa3 sendo Ka1, Ka2, Ka3, respectivamente, a primeira, segunda e terceira constantes de dissociação do ácido fosfórico.
b) As substâncias necessárias para preparar uma solução tampão de pH 7,4, dispondo-se do ácido fosfórico e respectivos sais de sódio. Justifique.
c) A razão molar das substâncias escolhidas no item b).
d) O procedimento experimental para preparar a solução tampão do item b).
Gabarito:
Resolução:
a)
Equações das reações de ionização das espécies ácidas e suas constantes de equilíbrio:
H3PO4 + H2O ⇌ H2PO4- + H3O+
Quando a fração das espécies for 0,5, a concentração de H2PO4- é igual a concentração de H3PO4. Portanto:
e
Tomando o -log dos dois lados da equação:
H2PO4- + H2O ⇌ HPO42- + H3O+
Quando a fração das espécies for 0,5, a concentração de HPO42- é igual a concentração de H2PO4-. Portanto:
e
Tomando o -log dos dois lados da equação:
HPO42- + H2O ⇌ PO43- + H3O+
Quando a fração das espécies for 0,5, a concentração de PO43- é igual a concentração de HPO42-. Portanto:
e
Tomando o -log dos dois lados da equação:
Analisando os valores de pH em cada um dos pontos em que a fração das espécies é 0,5, conclui-se que:
b)
Se o pH do meio for igual a 7, as espécies presentes no meio são H2PO4- e HPO42-. Podem ser utilizados os sais hidrogenofosfato de sódio (NaH2PO4) e hidrogenofosfato de sódio (Na2HPO4).
c)
Pela análise do gráfico, em pH = 7,4 as frações das espécies são aproximadamente 0,4 H2PO4- e 0,6 HPO42-.
d)
A partir das resoluções dos itens b e c, conclui-se que é necessário utilizar uma mistura de NaH2PO4 e Na2HPO4 na proporção molar de 2:3. Após pesadas as quantidades de sais, eles devem ser dissolvidos em água para formar a solução tampão.