Questão 6
ITA 2012
(ITA - 2012 - 2ª Fase)
Considere a reação de combustão do composto X, de massa molar igual a 27,7 g.mol-1, representada pela seguinte equação química balanceada:
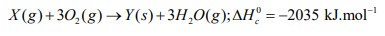
Calcule o valor numérico, em kJ, da quantidade de calor liberado na combustão de:
a) 1,0 x 103 g de X
b) 1,0 x 102 mol de X
c) 2,6 x 1022 moléculas de X
d) uma mistura de 10,0 g de X e 10,0 g de O2
Gabarito:
Resolução:
a) A partir da proporção estequiométrica, conclui-se que a cobustão de 1mol de X (27,7g) libera 2035 kJ. Portanto, a energia liberada na combustão de 1,0 x 103 g de X é:
| 27,7g X | __________ | -2035 kJ |
| 1,0 x 103 g X | __________ | a |
b) A partir da proporção estequiométrica, conclui-se que a cobustão de 1mol de X libera 2035 kJ. Portanto, a energia liberada na combustão de 1,0 x 102 mol de X é:
| 1mol X | __________ | -2035 kJ |
| 1,0 x 102 mol X | __________ | b |
b) A partir da proporção estequiométrica, conclui-se que a cobustão de 1mol de X (6,02 x 1023 moléculas) libera 2035 kJ. Portanto, a energia liberada na combustão de 2,6 x 1022 moléculas de X é:
| 6,02 x 1023 moléculas X | __________ | -2035 kJ |
| 2,6 x 1022 moléculas X | __________ | c |
d) Deve-se determinar qual é o reagente limitante e qual é o reagente em excesso. 1 mol de X (27,7g) reage completamente com 3 mol de O2 (96g).
• Cálculo da massa de X necessária para reagir completamente com 10,0g de O2:
| 27,7 g X | __________ | 96 g O2 |
| mX | __________ | 10 g O2 |
Portanto, o reagente X está em excesso.
A partir da proporção estequiométrica, conclui-se que na reação de 3 mol de O2 (96g) são liberados 2035 kJ de energia. Portanto, a energia liberada quando reagem 10,0g de O2 é:
| 96 g O2 | __________ | -2035 kJ |
| 10 g O2 | __________ | d |