Questão 28
ITA 2009
(ITA - 2009 - 2ª fase)
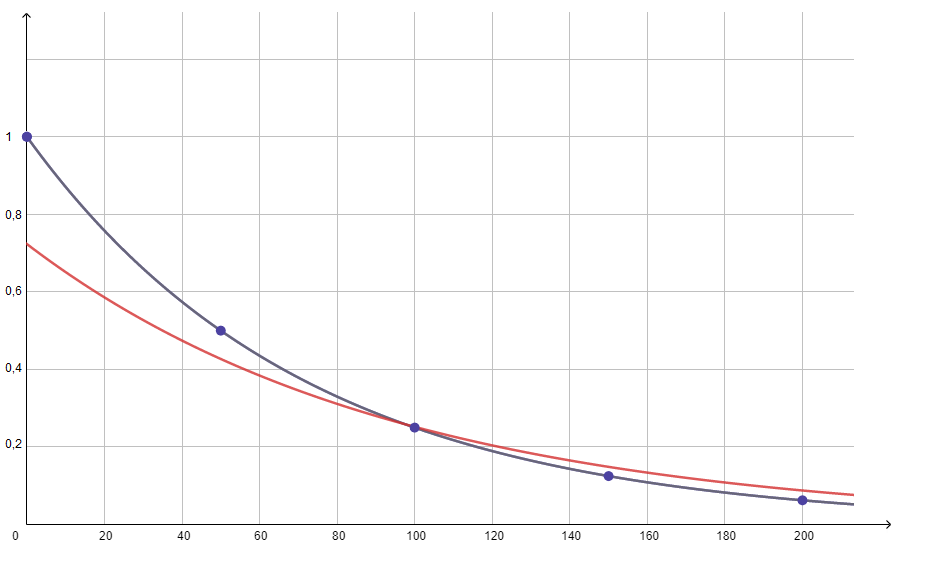
Considere duas reações químicas (I e II) envolvendo um reagente X. A primeira (I) é de primeira ordem em relação a X e tem tempo de meia-vida igual a 50 s. A segunda (II) é de segunda ordem em relação a X e tem tempo de meia-vida igual à metade da primeira reação. Considere que a concentração inicial de X nas duas reações é igual a 1,00 mol L-1. Em um gráfico de concentração de X (mol L-1) versus tempo (de 0 até 200 s), em escala, trace as curvas de consumo de X para as duas reações. Indique com I a curva que representa a reação de primeira ordem e, com II, a que representa a reação de segunda ordem.
Gabarito:
Resolução:
• Reação I
Lei de velocidade:
v = k[X]
para t = 0, [X] = 1,00 mol L-1
para t = 50, [X] = 0,500 mol L-1
para t = 100, [X] = 0,250 mol L-1
para t = 150, [X] = 0,125 mol L-1
para t = 200, [X] = 0,0625 mol L-1
• Reação II
Lei de velocidade:
v = k[X]2
Lei de velocidade integrada:
Como o tempo de meia vida é 25s, em t = 25s a concentração de X é metade da concentração inicial:
para t = 0, [X] = 1,00 mol L-1
para t = 50:
para t = 100:
para t = 150:
para t = 200: