Questão 28
ITA 2005
(ITA - 2005 - 2 FASE ) Considere uma reação química endotérmica entre reagentes, todos no estado gasoso.
A) ESBOCE graficamente como deve ser a variação da constante de velocidade em função da temperatura.
B) Conhecendo-se a função matemática que descreve a variação da constante de velocidade com a temperatura é possível determinar a energia de ativação da reação. EXPLIQUE como e JUSTIFIQUE.
C) DESCREVA um método que pode ser utilizado para determinar a ordem da reação.
Gabarito:
Resolução:
A) ESBOCE graficamente como deve ser a variação da constante de velocidade em função da temperatura.
O gráfico vai seguir a equação de Arrhenius:
Como temos uma exponencial, então o gráfico vai seguir uma exponencial. Quanto maior for a temperatura, menor será:
Logo, teremos um maior valor de:
E maior será o valor da constante de velocidade da reação. O gráfico será, então, uma exponencial que vai aumentar com o aumento da temperatura.
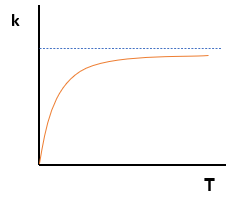
B) Conhecendo-se a função matemática que descreve a variação da constante de velocidade com a temperatura é possível determinar a energia de ativação da reação. EXPLIQUE como e JUSTIFIQUE.
Pela equação de Arrhenius, podemos calcular a energia de ativação:
Podemos obtê-la através da medição de valores experimentais de temperatura e a constante de velocidade da reação e, em seguida, linearizar os dados e fazer uma regressão:
C) DESCREVA um método que pode ser utilizado para determinar a ordem da reação.
A forma como o gráfico da linearização possuir vai informar a ordem da reação. Uma reação de ordem zero, por exemplo, forma uma reta.