Questão 9
ITA 2005
(ITA - 2005)
Considere as reações representadas pelas equações químicas a seguir:
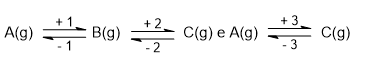
O índice positivo refere-se ao sentido da reação da esquerda para a direita e, o negativo, ao da direita para a esquerda. Sendo En energia de ativação e ∆H a variação de entalpia, são feitas as seguintes afirmações, todas relativas às condições-padrão:
I. ∆H+3 = ∆H+1 + ∆H+2
II. ∆H+1 = - ∆H-1
III. En+3 = En+1 + En+2
IV. En+3 = - En-3
Das afirmações acima está(ão) CORRETA(S)
Gabarito:
apenas I e II.
Resolução:
Analisando cada uma das afirmações:
I. Correta. A entalpia é uma função de estado, logo, depende apenas do estado inicial e do final. Por isso, é correto afirmar que ∆H+3 = ∆H+1 + ∆H+2, já que o estado inicial e final é o mesmo.
II. Correta. A entalpia da reaçãoo direta e inversa é igual, com a única diferença do sinal atribuído, portanto, ∆H+1 = - ∆H-1.
III. Incorreta. A energia de ativação não é função de estado, variando de acordo com a reação. Por isso, não é correto afirmar que a energia de ativação será a mesma se os reagentes e produtos forem iguais, independente do caminho.
IV. Incorreta. A energia de ativação da reação direta é diferente da reação inversa, já que os valores de entalpia são diferentes.
Como a questão pede apenas as corretas, a resposta é letra A.