Questão 88
ITA 2003
(ITA - 2003 - 1a fase)
Considere as seguintes espécies químicas no estado gasoso, bem como os respectivos átomos assinalados pelos algarismos romanos:
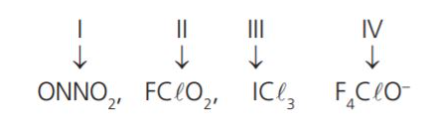
Os orbitais híbridos dos átomos assinalados por I, II, III e IV são respectivamente:
sp2, sp3, dsp3 e d2sp3.
sp2, sp2, sp3 e dsp3.
sp3, dsp3, d2sp3 e sp3.
sp3, sp2, dsp3 e d2sp3.
sp, dsp3, sp3 e dsp3.
Gabarito:
sp2, sp3, dsp3 e d2sp3.
Resolução:
I. A forma como está escrita a molécula de N2O3 → ONNO2 já nos dá uma dica de que o primeiro O está ligado à um N, que este está ligado ao outro N e que os outros dois O estão ligados à esse último N. Depois disso, lembramos de que N só pode fazer 3 lilgações covalentes, então uma das ligações com O deve ser dativa.
Como o N indicado possui 3 nuvens eletrônicas ao seu redor, temos uma hibridação sp².
Temos então as duas estruturas ressonantes:
II.
nº de valência: 7 + 7 + 6 + 6 = 26
Com todos os 26 elétrons distribuídos, temos 4 nuvens eletrônicas ao redor do Cloro, logo sua hibridação é sp3
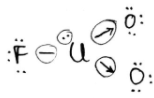
III.
º de valência: 7 + 7 + 7 + 7 = 28
Com todos os 28 elétrons distribuídos, temos 5 nuvens eletrônicas ao redor do Iodo, logo sua valência é sp3d
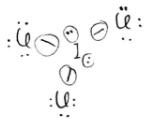
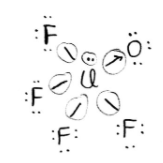
IV.
nº de valência: 7 + 7 + 7 + 7 + 7 + 6 + 1 = 42
Com todos os 42 elétrons distribuios, temos 6 nuvens eletrônicas ao redor do Cloro, logo sua hibridação é sp3d2