Questão 89
ITA 2003
(ITA - 2003 - 1a fase)
Na pressão de 1 atm, a temperatura de sublimação do CO2 é igual a 195 K. Na pressão de 67 atm, a temperatura de ebulição é igual a 298 K. Assinale a opção que contém a afirmação CORRETA sobre as propriedades do CO2.
A pressão do ponto triplo está acima de 1 atm.
A temperatura do ponto triplo está acima de 298 K.
A uma temperatura acima de 298 K e na pressão de 67 atm, tem-se que o estado mais estável do CO2 é o líquido.
Na temperatura de 195 K e pressões menores do que 1 atm, tem-se que o estado mais estável do CO2 é o sólido.
Na temperatura de 298 K e pressões maiores do que 67 atm, tem-se que o estado mais estável do CO2 é o gasoso.
Gabarito:
A pressão do ponto triplo está acima de 1 atm.
Resolução:
O diagrama de fases do dióxido de carbono é:
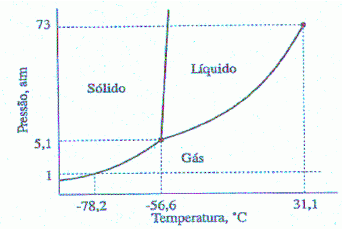
Analisando as alternativas:
A) A pressão do ponto triplo está acima de 1 atm.
CORRETO. Na pressão de 1 atm temos que o gás carbônico vai sublimar. Logo, o ponto triplo do dióxido de carbono deve estar em um valor acima de 1 atm.
B) A temperatura do ponto triplo está acima de 298 K.
INCORRETO. Como pode ser visto no diagrama de fases, o ponto triplo está abaixo de 298 K (25 ºC).
C) A uma temperatura acima de 298 K e na pressão de 67 atm, tem-se que o estado mais estável do CO2 é o líquido.
INCORRETO. A temperatura de ebulição do CO2, na pressão de 67 atm, é de 298 K. Logo, em uma temperatura acima de 298 K, seu estado mais estável será o gasoso.
D) Na temperatura de 195 K e pressões menores do que 1 atm, tem-se que o estado mais estável do CO2 é o sólido.
INCORRETO. Nessas condições, o CO2 sofre sublimação, transformando o CO2 sólido em gasoso. Logo, não teremos um estado mais estável.
E) Na temperatura de 298 K e pressões maiores do que 67 atm, tem-se que o estado mais estável do CO2 é o gasoso.
INCORRETO. Nesse caso, o CO2 está em ebulição, passando do estado líquido para o gasoso, sem nenhum estado estável.