Questão 95
ITA 2003
(ITA - 2003 - 1a fase)
Indique a opção que contém a equação química de uma reação ácido-base na qual a água se comporta como base.
NH3 + H2O NH4OH.
NaNH2 + H2O NH3 + NaOH.
Na2CO3 + H2O NaHCO3 + NaOH.
P2O5 + 3H2O 2H3PO4.
TiCℓ4 + 2H2O TiO2 + 4HCℓ.
Gabarito:
P2O5 + 3H2O 2H3PO4.
Resolução:
De acordo com a teoria ácido-base de Bronted-Lowry, ácido é a espécie que doa prótons, e base é a espécie que recebe prótons.
Já segundo Lewis, ácido é a espécie que recebe par de elétrons, e base é a espécie que doa par de elétrons.
Analisando cada uma das reações:
[A] Incorreta. H2O é um ácido.
NH3 + H2O ⇌ NH4OH
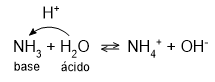
[B] Incorreta. H2O é um ácido.
NaNH2 + H2O ⇌ NH3 + NaOH
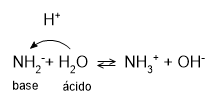
[C] Incorreta. H2O é um ácido.
Na2CO3 + H2O ⇌ NaHCO3 + NaOH
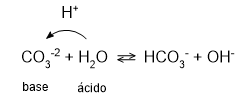
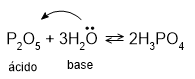
[D] Correta. H2O é uma base porque doa par de elétrons.
P2O5 + 3H2O ⇌ 2H3PO4
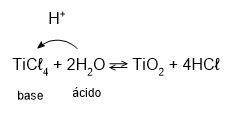
[E] Incorreta. H2O é um ácido.
TiCℓ4 + 2H2O ⇌ TiO2 + 4HCℓ