Questão 9314
ITA 2000
(ITA - 2000)
Considere os seguintes ácidos:
I. CH3COOH.
II. CH3CH2COOH.
III. CH2CCH2COOH.
IV. CHC2CH2COOH.
V. CC3CH2COOH.
Assinale a opção que contém a sequência CORRETA para a ordem crescente de caráter ácido:
I < II < III < IV < V.
II < I < III < IV < V.
II < I < V < IV < III.
III < IV < V < II < I.
V < IV < III < II < I.
Gabarito:
II < I < III < IV < V.
Resolução:
Para resolver essa questão é importante saber da influência do efeito indutivo doador e retirador na acidez de um composto orgânico.
O efeito indutivo retirador, ou seja, que retira densidade eletrônica, aumenta a carga parcial positiva no oxigênio ligado ao hidrogênio ácido, o que enfraquece a ligação O-H. Quanto mais fraca for a ligação, mais ácido é o composto, já que é mais fácil perder H+. Os principais grupos retiradores são os halogênios e o grupo nitro.
O efeito indutivo doador, ou seja, que doa densidade eletrônica, aumenta a carga parcial negativa do oxigênio ligado ao hidrogênio ácido, o que fortalece a ligação O-H. Quanto mais forte for a ligação, menos ácido é o composto, já que é mais difícil perder H+. Os principais grupos doadores são os grupos alquila.
Ambos os efeitos são somatórios, ou seja, quanto mais grupos retiradores estiverem presentes, mais fraca vai ser a ligação O-H e mais forte vai ser o ácido. E quanto mais grupos doadores estiverem presentes, mais forte vai ser a ligação O-H e mais fraco vai ser o ácido.
Portanto, para avaliar a acidez dos compostos das alternativas é importante analisar o efeito indutivo de cada um.
I) CH3COOH
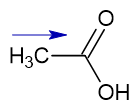
II) CH3CH2COOH
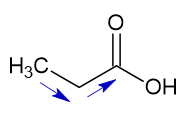
III) CH2CCH2COOH
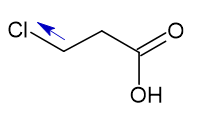
IV) CHC2CH2COOH
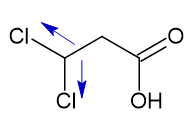
V) CC3CH2COOH
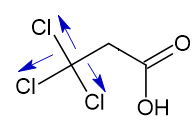
Portanto, a ordem crescente de acidez vai ser:
II < I < III < IV < V
Gabarito: alternativa B