Questão 9105
ITA 1999
(ITA 1999)
Considere que sejam feitas as seguintes afirmações em relação à pressão de vapor saturante de líquidos e/ou sólidos:
I - As pressões de vapor da água líquida e do gelo têm o mesmo valor a -10°C.
II - Tanto a pressão de vapor de líquidos como a de sólidos aumentam com o aumento da temperatura.
III - A pressão de vapor de um líquido depende das forças de interação intermoleculares.
IV - No ponto triplo da água pura, a pressão de vapor do gelo tem o mesmo valor que a pressão de vapor da água líquida.
V - A pressão de um vapor em equilíbrio com o respectivo líquido independe da extensão das fases gasosa e líquida.
Qual das opções a seguir se refere a todas afirmações CORRETAS?
I e II.
I e IV.
I, II, III e V.
II, III, IV e V.
I, II, III, IV e V.
Gabarito:
II, III, IV e V.
Resolução:
O gráfico a seguir representa a pressão de vapor da água em função da temperatura:
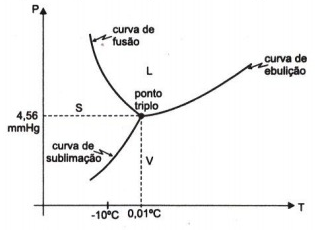
Analisando cada uma das afirmativas:
I ⇒ Incorreta. Em uma temperatura de -10ºC não coexistem líquido e vapor.
II ⇒ Correta. A pressão de vapor e a temperatura são diretamente proporcionais.
III ⇒ Correta. Quanto maior a interação intermolecular mais difícil é passar para o estado de vapor, então, menor a pressão de vapor.
IV ⇒ Correta. O ponto triplo é aquele no qual as três fases coexistem, então a pressão de vapor é a mesma. Isso pode ser observado no gráfico.
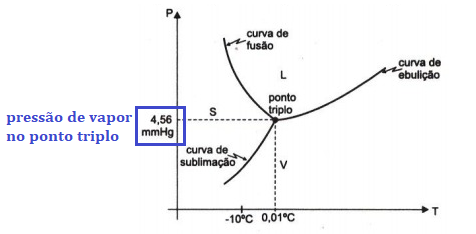
V ⇒ Correta. A pressão de vapor depende da temperatura e da natureza do líquido.
Gabarito: letra D