Questão 60479
INSPER 2019
O nitrogênio é o elemento mais abundante da atmosfera e faz parte de compostos essenciais para o sistema biológico, como aminoácidos e proteínas. Apesar de sua grande disponibilidade na forma de gás N2, poucas espécies são capazes de utilizá-lo dessa forma. Seu processo de transformação é denominado fixação e seu ciclo na natureza é representado na figura.
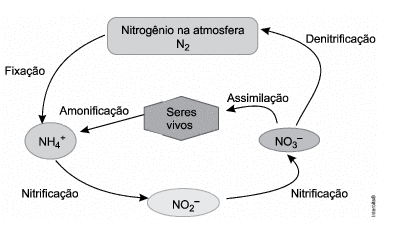
No ciclo do nitrogênio, a etapa que envolve oxidação é a
denitrificação, e são envolvidos 3 mol de elétrons para formação de 1 mol de N2 a partir do NO3-.
nitrificação, e são envolvidos 6 mol de elétrons para formação de 1 mol de NO2 – a partir do NH4+.
fixação do nitrogênio, e são envolvidos 3 mol de elétrons para formação de 1 mol de NH4+ a partir do N2.
fixação de nitrogênio, e são envolvidos 6 mol de elétrons para formação de 1 mol de NH4+ a partir do N2.
nitrificação, e são envolvidos 6 mol de elétrons para formação de 1 mol de NO3- a partir do NO2-.
Gabarito:
nitrificação, e são envolvidos 6 mol de elétrons para formação de 1 mol de NO2 – a partir do NH4+.
Resolução:
A etapa que envolve oxidação é a nitrificação, em que o NH4+ é transformado em NO2-.
Para calcular o número de oxidação do nitrogênio nessas espécies utiliza-se o nox conhecidos do hidrogênio (+1) e do oxigênio (-2) e o fato de que a soma do nox dos elementos multiplicados pelas respectivas atomicidades deve ser igual à carga da espécie.
Cálculo do número de oxidação do nitrogênio no NH4+:
Cálculo do número de oxidação do nitrogênio no NO2-:
Na formação do NO2- a partir do NH4+, o número de oxidação do nitrogênio varia de -3 para +3. Portanto, para a formação de 1mol de NO2- a partir do NH4+ são necessários 6mol de elétrons.