Questão 3
IME 2023
(IME - 2023/2024)
Durante um experimento em laboratório, o pesquisador verificou a necessidade de uma fonte de energia com capacidade de fornecer uma f.e.m. em corrente contínua com valor entre 2,0 e 2,5 volts. Para atender a essa demanda, decidiu montar uma pilha eletroquímica, tendo disponíveis ácido sulfúrico, estanho, magnésio e níquel, e utilizou um circuito sempre fechado em que não se aplica o Princípio de Le Chatelier.
Potenciais-padrão de redução com base no eletrodo padrão de hidrogênio:
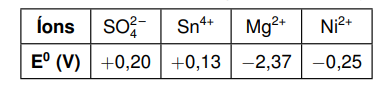
Com base nas informações acima, pede-se:
a) identificar os elementos que o pesquisador deve selecionar para compor a pilha;
b) mostrar que a f.e.m. da pilha selecionada atende à necessidade do experimento;
c) escrever as semirreações e a reação global para a pilha selecionada.
Gabarito:
Resolução:
Para selecionar quais materiais devem compor a pilha, basta analisar a f. e. m. fornecida por cada par, por meio da equação
a) Sendo assim, os pares Mg+2 e Sn+4 (fonece 2,5V) e Mg+2 e Ni+2 (fornece 2,12V) atendem ao requerido pelo pesquisador, mas, como o valor deve estar entre 2,0V e 2,5V, a pilha deve ser formada pelo segundo par.
b) Conforme dito anteriormente, é possível calcular a f. e. m. a partir da equação descrita, dessa forma,
c) As semirreações estão descritas abaixo
Oxidação:
, Eº = -0,25V
Redução:
, Eº = -2,37V
Somando as duas reações, encontra-se a reação global.
, Eº = 2,12V