Questão 82024
IME 2023
O cálcio metálico reage com hidrogênio gasoso para produzir hidreto metálico. A pressão de equilíbrio do hidrogênio gasoso em função do inverso da temperatura absoluta dessa reação segue o gráfico a seguir.
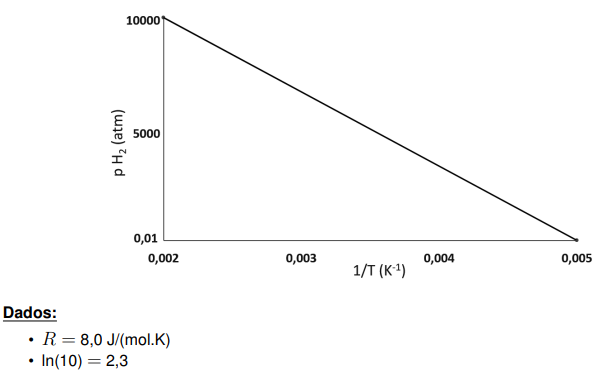
O calor, em kJ, envolvido na produção de 1 mol desse hidreto, a pressão constante de 1 atm, considerando comportamento de gás ideal, é aproximadamente igual a:
− 37
− 25
0
+ 25
+ 37
Gabarito:
− 37
Resolução:
Para a reação, a constante de equilíbrio é 1/PH2, dessa forma, pela Equação de Van't Hoff, temos,
Tomando dois pontos no gráfico (0,002;10000) e (0,005; 0,01), é obtido:
lnP1 = 2,3 . 4 = 9,2
lnP2 = 2,3 . (-2) = -4,6
Logo,
Com o aumento de temperatura, a pressão é aumentada no equilíbrio, a reação é exotérmica e o valor é negativo.