Questão 10
IME 2016
[IME-2016/2017 - 2ª fase]
A técnica de Osmometria de Pressão de Vapor (OPV) permite determinar a massa molar de uma substância desconhecida através da quantificação da diferença de temperatura (T) entre uma gota de solução diluída da substância desconhecida e uma gota do solvente puro utilizado nesta diluição, em câmara saturada com o mesmo solvente, conforme o dispositivo abaixo.
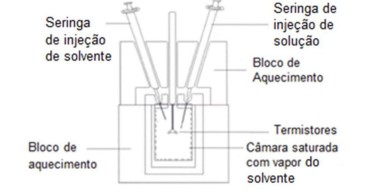
A diferença de temperatura (T) tem relação direta com o abaixamento da pressão de vapor (
P), conforme a expressão:
em que R = constante universal dos gases ideais, T0 = temperatura de ebulição do solvente puro, P0 = pressão de vapor do solvente puro e Hvap = entalpia de vaporização do solvente puro. Demonstre que, segundo a técnica de OPV, a massa molar M1 de uma substância desconhecida pode ser quantificada por:
em que M0 = massa molar do solvente e W1 = fração mássica do soluto desconhecido na solução diluída.
Gabarito:
Resolução:
Expressão fornecida no enunciado:
(equação 1)
Essa equação pode ser reescrita como
(equação 2)
Pela Lei de Raoult, a pressão parcial de um componente i na solução (pi) é a multiplicação entre pressão parcial do componente i puro (p*i) e a fração molar de i (xi)
A pressão de vapor total da solução é a soma das pressões parciais dos componentes. O sistema em questão é formado por dois líquidos, então a pressão de vapor da solução é
Como o soluto é não-volátil, sua pressão parcial é zero. Portanto, a pressão de vapor da solução é igual à pressão de vapor do solvente
A adição de um soluto não volátil diminui a pressão de vapor do solvente. Essa variação de pressão é dada por
(equação 3)
A soma das frações molares dos componentes é igual a 1
Portanto, pode-se substituir o termo (1-x0) na equação 3:
(equação 4)
A fração molar do componente 1 é a razão entre a quantidade de matéria de 1 e a quantidade de matéria total:
(equação 5)
A quantidade de matéria total é a soma das quantidades de matéria dos dois componentes:
Como a solução é muito diluída, pode-se fazer a aproximação de que a quantidade de matéria total é igual à quantidade de matéria do solvente
A massa molar é a razão entre a massa e a quantidade de matéria
E a quantidade de matéria é a razão entre a massa e a massa molar
(equação 6)
Substituição da equação 6 na equação 5:
(equação 7)
A fração mássica é a razão entre a fração do componente 1 e a massa total da mistura:
Novamente, como a solução é muito diluída, pode-se aproximar a massa total como sendo a massa do solvente:
Portanto:
(equação 8)
Substituição da equação 8 na equação 7:
(equação 9)
Substituição da equação 9 na equação 4:
(equação 10)
Substituição da equação 10 na equação 2:
Resolve-se a equação para M1: