Questão 34
IME 2015
|
QUESTÃO ANULADA!!! [IME-2015 / 2016 - 1 fase] |
A escolha de um indicador eficaz deve ser feita de acordo com a natureza do ácido e da base utilizados em uma titulação. As substâncias que atuam como indicadores ácido-base são corantes que mudam de cor em faixas estreitas de pH e, na maioria das vezes, são ácidos fracos. Dado um indicador HA, um ácido monoprótico fraco, verifica-se que sua cor no estado não-ionizado é nitidamente diferente da cor de sua base conjugada A−. Se o indicador estiver em meio suficientemente ácido, o equilíbrio desloca-se de acordo com o princípio de Le Chatelier e a cor predominante é a da forma não-ionizada, HA. Em meio suficientemente básico, ocorre o inverso, ou seja, o equilíbrio desloca-se de modo a prevalecer a cor da base conjugada A−. Considere que, de modo aproximado, possam ser utilizados os seguintes quocientes entre concentrações para prever a cor que o indicador vai apresentar:

Com base nestes dados, e sabendo que HA tem constante de ionização igual a , é coerente afirmar que o indicador HA
(Dado: log 4 = 0,6)
a) é adequado para uma titulação de 0,10M por NaOH 0,10M
b) é adequado para uma titulação de NH3 0,10 M por HCl 0,10M.
c) muda de cor quando a solução em que se encontra muda de ácida para básica ou vice-versa.
d) quando se atinge pH = 10,4, inicia-se a transição de cor em uma titulação de NaOH por CH3COOH.
e) quando o pH é igual a 8,0, prevalece a cor de A− em uma titulação de NaOH por CH3COOH.
QUESTÃO ANULADA!!!
Próxima questão
Marque a letra A
Gabarito:
Próxima questão
Resolução:
Para um ácido monoprótico fraco (HA) vem:
Aplicando -log para os dois lados:
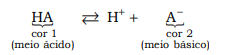
Para HClO4 e NaOH é possível a utilização do HA como indicador. Para o pH igual a 10,4, começa uma mudança de cor em uma titulação de uma base forte por ácido fraco. Não há resposta correta.