Questão 3
FUVEST 2022
(FUVEST - 2022 - 2ª FASE)
As afirmações a seguir baseiam-se na descrição da CETESB (Companhia Ambiental do Estado de São Paulo):
Afirmação 1: “O dióxido de enxofre (SO2) é liberado para a atmosfera por gases vulcânicos e fontes antropogênicas, principalmente atividades industriais que processam materiais contendo enxofre, como termelétricas, fabricação de fertilizantes, fundição de alumínio e aço, produção de ácido sulfúrico e papel.”
Afirmação 2: “O dióxido de enxofre é um gás incolor com forte odor pungente. É muito irritante quando em contato com superfícies úmidas, pois se transforma em trióxido de enxofre (SO3) e passa rapidamente a ácido sulfúrico (H2SO4).”
a) Represente a estrutura de Lewis do dióxido de enxofre.
b) A afirmação 2 refere-se à formação da chuva ácida. Represente a reação balanceada da formação da chuva ácida a partir de SO3 e a reação balanceada da chuva ácida com o carbonato de cálcio (CaCO3), que é um dos componentes de construções que são danificadas por ela.
c) Considere uma determinada amostra de carvão que contém 1% em massa de enxofre. Quando esse carvão é queimado, o enxofre é convertido em dióxido de enxofre pela reação S(s) + O2(g)→ SO2(g). Para evitar a poluição do ar, este dióxido de enxofre pode ser tratado com óxido de cálcio para formar sulfito de cálcio, como representado pela reação SO2(g) + CaO(s) → CaSO3(s). Calcule a massa diária, em quilogramas, de CaO necessária para tratar o SO2 em uma usina que consome 3,2 × 106 kg de carvão por dia.
|
Note e adote: Distribuição eletrônica: O = 1s2, 2s2, 2p4; S = 1s2, 2s2, 2p6, 3s2, 3p4. Massas molares (g/mol): O = 16; S = 32; Ca = 40 |
Gabarito:
Resolução:
a)
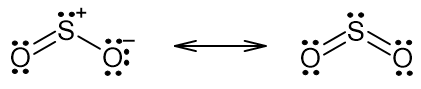
b)
• Equação da reação da formação da chuva ácida a partir de SO3:
SO3(g) + H2O(l) → H2SO4(aq)
• Equação da reação da chuva ácida com o carbonato de cálcio:
A reação entre o ácido sulfúrico (H2SO4) e o carbonato de cálcio forma sulfato de cálcio (CaCO3) e ácido carbônico (H2CO3). O ácido carbônico é instável e se decompõe em dióxido de carbono (CO2) e água (H2O).
H2SO4(aq) + CaCO3(s) → CaSO4(s) + CO2(g) + H2O(l)
c)
• Cálculo da massa de enxofre em 3,2 x 106 kg de carvão:
| 100g de carvão | __________ | 1g de S |
| 3,2 x 106 kg de carvão | __________ | mS |
A reação descrita ocorre em duas etapas:
1) S(s) + O2(g)→ SO2(g)
2) SO2(g) + CaO(s) → CaSO3(s)
Para cada 1mol de S consumido, forma-se 1mol de SO2. Para tratar cada 1mol de SO2 é necessário 1mol de CaO. Portanto, pode-se calcular a massa de CaO necessária para tratar 32g de enxofre a partir da proporção:
| 1mol de S | __________ | 1mol de CaO |
| 32g de S | __________ | 56g de CaO |
| 32000 kg de S | __________ | mCaO |