Questão 71
FUVEST 2022
(FUVEST- 2022 - 1ª fase)
Oxigênio (O2) e ozônio (O3) estão em constante processo de consumo e produção na estratosfera, como representado pelas equações químicas a seguir. As reações I e II ilustram etapas da produção de ozônio a partir de oxigênio, e a reação III mostra a restauração de oxigênio a partir de ozônio.
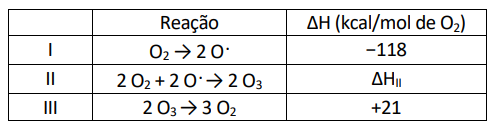
O ΔHII, relacionado à reação II, pode ser calculado a partir dos dados fornecidos para as reações I e III. O valor de ΔHII, em kcal/mol de O2 consumido, é igual a:
−90,5
−55,0
+27,5
+48,5
+55,0
Gabarito:
+27,5
Resolução:

Equações das reações I e III apresentadas na tabela do enunciado:
| I. O2 → 2 O• | ΔHI = -118 |
| III. 2 O3 → 3 O2 | ΔHIII = +21 |
A equação da reação II é obtida invertendo a equação das reações I e III e somando-as:
• Inversão das equações
| 2 O• → O2 | ΔH-I = +118 |
| 3 O2 → 2 O3 | ΔH-III = 3 x (-21) |
• Soma das equações:
| 2 O• + 3 O2 → O2 + 2 O3 | ΔHII = +118 + 3 x (-21) |
• Simplificação:
| 2 O• + 2 O2 → 2 O3 | ΔHII = +118 + 3 x (-21) |
Portanto, o ΔHII pode ser calculado utilizando a seguinte equação:
ΔHII = -ΔHII + 3 x (-ΔHIII)
Substituição dos valores das variações de entalpia das reações I e II:
ΔHII = 118 + 3 x (-21)
ΔHII = 118 - 63
ΔHII = 55 kJ
Entretanto, esse valor corresponde à entalpia da reação em que são consumidos 2 mol de O2. Calcula-se a entalpia da reação em que 1mol de O2 é consumido pela relação
| 2 mol O2 | 55 kJ |
| 1 mol O2 | ΔHII' |
Portanto, o valor da entalpia da reação II, em kcal/mol de O2 consumido, é igual a:
ΔHII' = 27,5 kJ/mol