Questão 44591
FUVEST 2009
(FUVEST - 2009 - 2 fase - Questão 1)
Água pode ser eletrolisada com a finalidade de se demonstrar sua composição. A figura representa uma aparelhagem em que foi feita a eletrólise da água, usando eletrodos inertes de platina.
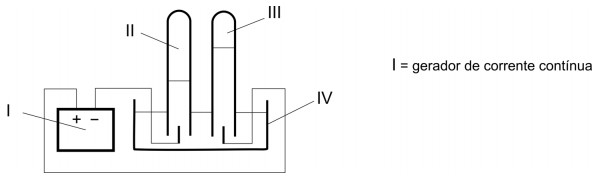
a) Nesse experimento, para que ocorra a eletrólise da água, o que deve ser adicionado, inicialmente, à água contida no recipiente IV? Justifique.
b) Dê as fórmulas moleculares das substâncias recolhidas, respectivamente, nos tubos II e III.
c) Qual a relação estequiométrica entre as quantidades de matéria (mols) recolhidas em II e III?
d) Escreva a equação balanceada que representa a semi-reação que ocorre no eletrodo (anodo) inserido no tubo III.
Gabarito:
Resolução:
a) Para que haja condução de corrente elétrica, é necessária a presença de íons livres na solução. No caso, para fazermos a eletrólise da água, devemos adicionar no recipiente
IV um eletrólito, sendo que o cátion deve possuir potencial de redução menor que o da água, assim como para o ânion.
b) No catodo ocorre redução da água de acordo com a equação abaixo:
2H2O(l) + 2e– → H2(g) + 2OH–(aq)
No anodo ocorre oxidação da água:
H2O(l) → 2H+(aq) + 1/2O2(g) + 2e–
As fórmulas das substâncias recolhidas nos tubos II e III são, respectivamente, H2 e O2.
c) A equação global da eletrólise da água é
H2O → H2 + 1/2 O2
A proporção entre H2 e O2 é de 1 mol de H2 para 0,5 mol de O2, ou seja, temos uma proporção de 2:1.
d) H2O(l) → 2H+(aq) + 1/2 O2(g) + 2e–