Questão 10585
FUVEST 2007
(FUVEST - 2007 - 1a fase)
A figura mostra modelos de algumas moléculas com ligações covalentes entre seus átomos.
Analise a polaridade dessas moléculas, sabendo que tal propriedade depende da
- diferença de eletronegatividade entre os átomos que estão diretamente ligados. (Nas moléculas apresentadas, átomos de elementos diferentes têm eletronegatividades diferentes.)
- forma geométrica das moléculas.
(Observação: Eletronegatividade é a capacidade de um átomo para atrair os elétrons da ligação covalente.)
Dentre essas moléculas, pode-se afirmar que são polares apenas
A e B.
A e C.
A, C e D.
B, C e D.
C e D.
Gabarito:
C e D.
Resolução:
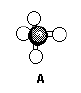
Geometria: tetraédrica
Apresenta quatro ligantes iguais, logo, trata-se de uma molécula apolar.
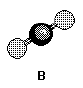
Geometria: linear
Apresenta dois átomos iguais ligados ao átomo central, como sua geometria é linear, a diferença de eletronegatividade se anula. Molécula apolar.
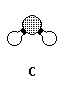
Geometria: angular.
Possui dois átomos iguais ligados ao átomo central. Como sua geometria é angular, a diferença de eletronegatividade não vai se anular, tendo uma resultante (neste caso) para cima. Molécula Polar.
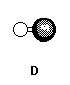
Molécula diatômica (dois átomos), formada por átomos de elementos diferentes, portanto, é polar.
Gabarito alternativa E.