Questão 73
FUVEST 2004
(FUVEST - 2004 - 1a fase)
A transformação de um composto A em um composto B, até se atingir o equilíbrio , foi estudada em três experimentos. De um experimento para o outro, variou-se a concentração inicial do reagente A ou a temperatura ou ambas. Registraram-se as concentrações de reagente e produto em função do tempo.
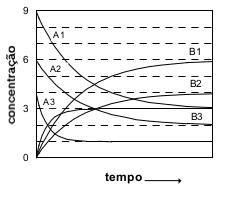
Com esses dados, afirma-se:
I. Os experimentos 1 e 2 foram realizados à mesma temperatura, pois as constantes de equilíbrio correspondentes são iguais.
II. O experimento 3 foi realizado numa temperatura mais elevada que o experimento 1, pois no experimento 3 o equilíbrio foi atingido em um tempo menor.
III. A reação é endotérmica no sentido da formação do produto B.
Dessas afirmações,
todas são corretas.
apenas I e III são corretas.
apenas II e III são corretas.
apenas I é correta.
apenas II é correta.
Gabarito:
todas são corretas.
Resolução:
Calculando com os dados do gráfico, encontramos que a constante de equilíbrio para cada experimento é
K1=K2=2 e K3=3
Item I: Correto.
Devido à dependência da constante de equilíbrio em relação à temperatura, é possível concluir que os experimentos 1 e 2 foram realizados à mesma temperatura.
Item II: Correto.
A partir da análise do gráfico, observamos que o equilíbrio foi alcançado de forma mais rápida no experimento 3. Concluímos, portanto, que essa experimentação ocorreu em uma temperatura mais elevada, uma vez que o aumento da temperatura resulta em maior velocidade da reação, reduzindo o tempo necessário para atingir o equilíbrio.
Item III: Correto.
Em uma reação endotérmica, o aumento da temperatura desloca o equilíbrio em direção à formação de produtos, aumentando numericamente o valor da constante de equilíbrio.