Questão 12
ESPCEX 2020
(EsPCEx - 2020)
Nestes últimos anos, os alunos da EsPCEx têm realizado uma prática no laboratório de química envolvendo eletrólises com eletrodos inertes de grafite. Eles seguem um procedimento experimental conforme a descrição:
- Num béquer de capacidade 100mL (cuba eletrolítica) coloque cerca de 50mL de solução aquosa de sulfato de zinco (ZnSO4) de concentração 1molL-1. Tome como eletrodos duas barras finas de grafite. Ligue-as com auxílio de fios a uma fonte externa de eletricidade (bateria) com corrente de 2 Ampères. Esta fonte tem capacidade para efetuar perfeitamente esse processo de eletrólise. Uma das barras deve ser ligada ao polo negativo da fonte e a outra barra ao polo positivo da fonte. Mergulhe os eletrodos na solução durante 32 minutos e 10 segundos e observe.
Considere o arranjo eletrolítico (a 25ºC e 1atm), confirme visto na figura a seguir:
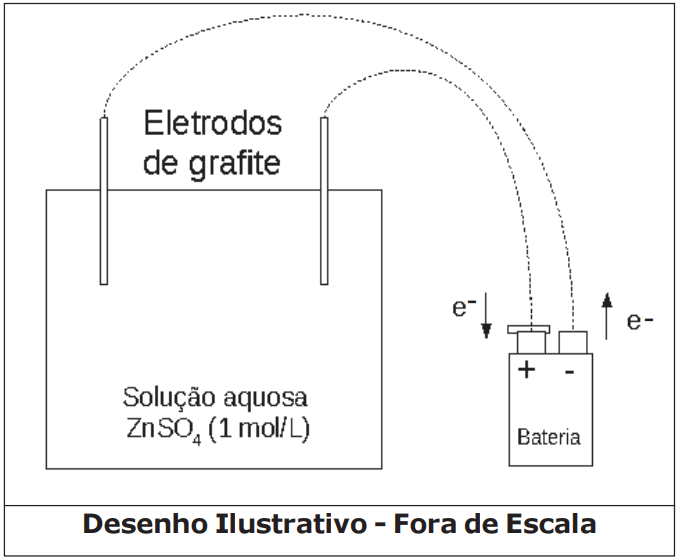
Dados: 1 Faraday (F) = 96500 Coulomb (C) / mol de elétrons.
Acerca do experimento e os conceitos químicos envolvidos são feitas as seguintes afirmativas:
I - Na superfície da barra de grafite ligada como cátodo da eletrólise ocorre a eletrodeposição do zinco metálico.
II - A semirreação de oxidação que ocorre no ânodo da eletrólise é Zn(s) → Zn+2(aq) + 2e-.
III - Durante o processo a barra de grafite ligada ao polo positivo da bateria se oxida.
IV - No ânodo da eletrólise ocorre uma reação de oxidação da hidroxila com formação do gás oxigênio e água.
V - A massa de zinco metálico obtida no processo de eletrólise será de 0,83g.
Das afirmativas feitas, estão corretas apenas
I e IV.
I, III e IV.
I e V.
II e III.
III, IV e V.
Gabarito:
I e IV.
Resolução:
Em uma eletrólise, o polo positivo é o ânodo e é nele que ocorre a oxidação, ou seja, doação de elétrons. Já o polo negativo é o cátodo, e nele ocorre a redução. Portanto, o fluxo de elétrons é do ânodo para o cátodo:
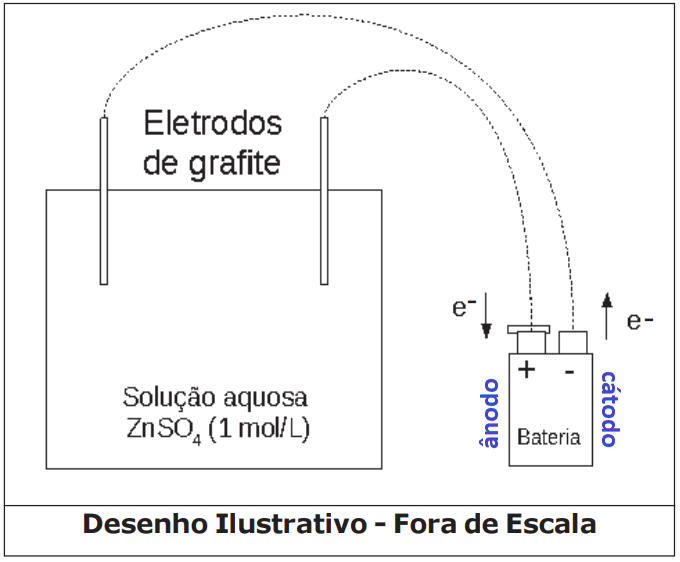
Na imagem o fluxo de elétrons está invertido, mas é possível identificar os eletrodos pelo sinal e esse dado não é importante para a resolução do restante da questão.
Na eletrólise aquosa do ZnSO4, vão ocorrer as seguintes reações químicas:
Dissociação do ZnSO4 ⇒ ZnSO4 → Zn+2 + SO4-2
Ionização da água ⇒ 2 H2O → H3O+ + OH-
Para o polo positivo (ânodo) serão direcionados as cargas negativas, ou seja, SO4-2 e OH-. Dentre esses, o OH- tem maior facilidade de descarga (vide imagem) e por isso irá oxidar.
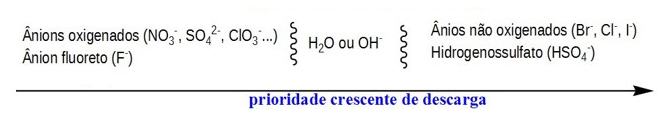
A reação de oxidação do OH- pode ser representada pela equação:
4 OH- → 2 H2O + O2 + 4 e-
Já no polo negativo (cátodo) estarão as cargas positivas, ou seja, Zn+2 e H+. Dentre esses, o Zn+2 tem maior facilidade de descarga (vide imagem) e por isso irá reduzir.
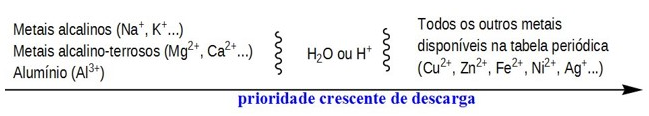
A reação de redução do Zn+2 pode ser representada pela equação:
Zn+2 + 2 e- → Zn
Somando todas as reações que ocorrem nessa célula, a equação global será:
2 ZnSO4 + 6 H2O → 2 Zn + O2 + 4 H3O+ + 2 SO4-2
Tendo feito a intepretação inicial, passamos para a análise de cada uma das afirmativas:
I - Verdadeira. O zinco sofre redução no cátodo, passando de Zn+2 para Zn.
II - Falsa. A espécie que sofre oxidação é o OH-, sendo representado pela equação 4 OH- → 2 H2O + O2 + 4 e-.
III - Falsa. Os eletrodos de grafite são eletrodos inertes, ou seja, não participam da reação de oxirredução.
IV - Verdadeira. A reação de oxidação que ocorre no ânodo é representada por 4 OH- → 2 H2O + O2 + 4 e-.
V - Falsa. Para calcular a massa de zinco, considerando os dados fornecidos de corrente e tempo, é utilizada a fórmula:
Sendo, m = massa (g) ; i = corrente (A) ; t = tempo (s) ; E = equivalente-grama.
O equivalente-grama é calculado pela fórmula:
sendo, M = massa molecular ; k = número de elétrons envolvidos.
Então, o equivalente grama do zinco será:
Substituindo todos os valores na primeira equação:
Considerando apenas as alternativas verdadeiras, gabarito letra A.