Questão 20
ESPCEX 2010
(EsPCEx - 2010)
O íon nitrato (NO3-), a molécula de amônia (NH3) , a molécula de dióxido de enxofre (SO2) e a molécula de ácido bromídrico (HBr) apresentam, respectivamente, a seguinte geometria:
| Elemento químico |
N (Nitrogênio) |
O (Oxigênio) | H (hidrogênio) | S (enxofre) | Br (bromo) |
| Número atômico (Z) | 7 | 8 | 1 | 16 | 35 |
piramidal; trigonal plana; linear; angular.
trigonal plana; piramidal; angular; linear.
piramidal; trigonal plana; angular; linear.
trigonal plana; piramidal; trigonal plana; linear.
piramidal; linear; trigonal plana; tetraédrica.
Gabarito:
trigonal plana; piramidal; angular; linear.
Resolução:
As moléculas tendem à adquirir geometrias em que as repulsões entre os pares de elétrons seja minimizada.
Essas são as estruturas de cada uma dessas espécies e suas respectivas geometrias:
Nitrato (NO3-)
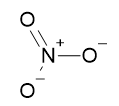
O nitrogênio possui três ligantes e não possui pares de elétrons não ligantes. A geometria em que os três átomos de oxigênio estão mais afastados uns dos outros é a trigonal plana.
Amônia (NH3)
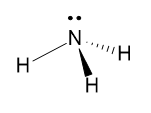
A amônia possui três ligantes e um par de elétrons não ligantes. Existe uma repulsão entre esse par de elétrons e os elétrons das ligações N-H. A geometria em que essa repulsão é minimizada é a piramidal.
Dióxido de enxofre (SO2)
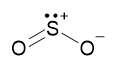
O enxofre possui dois ligantes e um par de elétrons não ligantes. Existe uma repulsão entre esse par de elétrons e os elétrons das ligações S-O. A geometria em que essa repulsão é minimizada é a angular.
Ácido bromídrico (HBr)
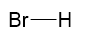
Qualquer molécula formada por apenas dois átomos tem geometria linear.