Questão 122
ENEM 2022
(ENEM - 2022)
O ácido tartárico é o principal ácido do vinho e está diretamente relacionado com sua qualidade. Na avaliação de um vinho branco em produção, uma analista neutralizou uma alíquota de 25,0 mL do vinho com NaOH a 0,10 mol L-1, consumindo um volume igual a 8,0 mL dessa base. A reação para esse processo de titulação é representada pela equação química:
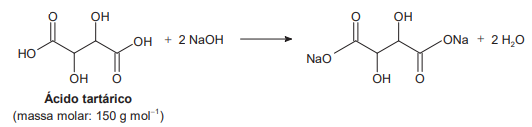
A concentração de ácido tartárico no vinho analisado é mais próxima de:
1,8 g L-1
2,4 g L-1
3,6 g L-1
4,8 g L-1
9,6 g L-1
Gabarito:
2,4 g L-1
Resolução:
Quantidade de base utilizada é:
V = 8,0 mL com concentração de 0,10 mol/L
Como a proporção de ácido e base descrita na reação é de 2 mol de base para 1 mol de ácido, então a quantidade de ácido neutralizada pela base é de:
y = 0,0004 mol de ácido
O volume no qual havia essa quantidade de ácido era o volume de 25mL, para calcular a concentração em mol/L:
Convertendo a quantidade de mol para grama temos (MMácido = 150gmol-1):
M = 2,4g
Como esses 2,4g estão em 1 litro de solução, portanto, a concentração é de 2,4g/L