Questão 113
ENEM 2020
(ENEM PPL 2020) Tanto a conservação de materiais biológicos como o resfriamento de certos fotodetectores exigem baixas temperaturas que não são facilmente atingidas por refrigeradores. Uma prática comum para atingi-las é o uso de nitrogênio líquido, obtido pela expansão adiabática do gás N2, contido em um recipiente acoplado a um êmbolo, que resulta no resfriamento em temperaturas que chegam até seu ponto de liquefação em −196 °C. A figura exibe o esboço de curvas de pressão em função do volume ocupado por uma quantidade de gás para os processos isotérmico e adiabático. As diferenças entre esses processos podem ser identificadas com base na primeira lei da termodinâmica, que associa a variação de energia interna à diferença entre o calor trocado com o meio exterior e o trabalho realizado no processo.
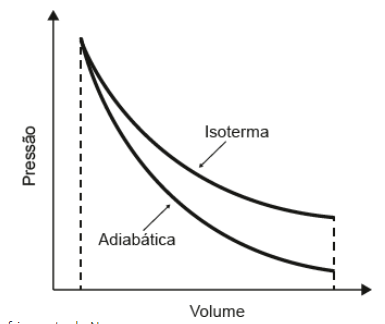
A expansão adiabática viabiliza o resfriamento do N2 porque
a entrada de calor que ocorre na expansão por causa do trabalho contribui para a diminuição da temperatura.
a saída de calor que ocorre na expansão por causa do trabalho contribui para a diminuição da temperatura.
a variação da energia interna é nula e o trabalho é associado diretamente ao fluxo de calor, que diminui a temperatura do sistema.
a variação da energia interna é nula e o trabalho é associado diretamente à entrada de frio, que diminui a temperatura do sistema.
o trabalho é associado diretamente à variação de energia interna e não há troca de calor entre o gás e o ambiente.
Gabarito:
o trabalho é associado diretamente à variação de energia interna e não há troca de calor entre o gás e o ambiente.
Resolução:
Transformações adiabáticas são aquelas que ocorrem de maneira a não permitir que o gás troque calor com o meio externo. Portanto, na Primeira Lei da Termodinâmica, vamos ter Q = 0:
Como interpretamos essa expressão?
O que essa equação nos diz é que toda energia utilizada para realizar trabalho pelo gás é retirada diretamente do grau de agitação das moléculas do gás. Ora, se o gás não pode trocar calor com o ambiente e este realiza trabalho, essa energia deve vir de algum lugar, correto? E a resposta é que o gás cede (ou aumenta) sua própria energia interna, a fim de tornar possível a realização de trabalho.
Portanto, como isso se aplica no exercício?
O que essa questão esperava do candidato era que ele associasse o resfriamento rápido ao trabalho positivo. Veja, se o trabalho do nitrogênio é positivo (expansão) teremos:
Portanto, a variação da energia interna será negativa, resultante um resfriamento súbito do gás enquanto este é comprimido. Assim, o trabalho é associado diretamente à variação de energia interna e não há troca de calor entre o gás e o ambiente. Caracterizando a alternativa E.
Erro das outras alternativas:
a) Não há entrada de calor se a transformação é adiabática;
b) Não há saída de calor se a transformação é adiabática;
c) Se o nitrogênio está alterando sua temperatura através de uma transformação adiabática não é possível que a variação de energia interna seja nula;
d) A variação da energia interna não é nula, como visto em (c);