Questão 121
ENEM 2019
(ENEM PPL - 2019)
Laboratórios de química geram como subprodutos substâncias ou misturas que, quando não têm mais utilidade nesses locais, são consideradas resíduos químicos. Para o descarte na rede de esgoto, o resíduo deve ser neutro, livre de solventes inflamáveis e elementos tóxicos como Pb, Cr e Hg. Uma possibilidade é fazer uma mistura de dois resíduos para obter um material que apresente as características necessárias para o descarte. Considere que um laboratório disponha de frascos de volumes iguais cheios dos resíduos, listados no quadro.
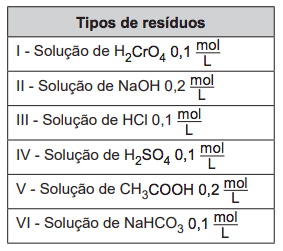
Qual combinação de resíduos poderá ser descartada na rede de esgotos?
I e II
II e III
II e IV
V e VI
IV e VI
Gabarito:
II e IV
Resolução:
I. Solução de H2CrO4 0,1mol.L-1
II. Solução de NaOH 0,2mol.L-1
III. Solução de HCl 0,1mol.L-1
IV. Solução de H2SO4 0,1mol.L-1
V. Solução de CH3COOH 0,2mol.L-1
VI. Solução de NaHCO3 0,1mol.L-1
O resíduo deve ser neutro, livre de solventes inflamáveis e elementos tóxicos como Pb, Cr e Hg.
a) Incorreta. I e II: solução de H2CrO4 0,1mol.L-1 + solução de NaOH 0,2mol.L-1
O resíduo possui crômio (H2CrO4).
b) Incorreta. II e III: solução de NaOH 0,2mol.L-1 + solução de HCl 0,1mol.L-1
Equação balanceada da reação entre hidróxido de sódio e ácido clorídrico:
NaOH + HCl → NaCl + H2O
A proporção entre os reagentes é de 1:1. Portanto, ao se misturar volumes iguais, essa solução será neutra se as concentrações dos reagentes forem iguais. Como a concentração do hidróxido de sódio é o dobro da concentração do ácido clorídrico, essa solução não é neutra.
c) Correta. II e IV: solução de NaOH 0,2mol.L-1 + solução de H2SO4 0,1mol.L-1
Equação balanceada da reação entre hidróxido de sódio e ácido sulfúrico:
2 NaOH + H2SO4 → Na2SO4 + 2 H2O
A proporção entre os reagentes é de 1:2. Portanto, ao se misturar volumes iguais, essa solução será neutra se a concentração de NaOH for o dobro da concentração de H2SO4. Como a concentração do hidróxido de sódio é o dobro da concentração do ácido sulfúrico, essa solução é neutra e esse resíduo pode ser descartado na rede de esgotos.
d) Incorreta. V e VI: solução de CH3COOH 0,2mol.L-1 + solução de NaHCO3 0,1mol.L-1
Equação balanceada da reação entre o ácido acético e o bicarbonato de sódio:
CH3COOH + NaHCO3 → CH3COONa + H2O + CO2
A proporção entre os reagentes é de 1:1. Portanto, ao se misturar volumes iguais, essa solução será neutra se as concentrações dos reagentes forem iguais. Como a concentração do ácido acético é o dobro da concentração do bicarbonato de sódio, essa solução não é neutra.
e) Incorreta. IV e VI: IV. Solução de H2SO4 0,1mol.L-1 + solução de NaHCO3 0,1mol.L-1
Equação balanceada da reação entre o ácido sulfúrico e bicarbonato de sódio
H2SO4 + 2 NaHCO3 → Na2SO4 + 2 H2O + CO2
A proporção entre os reagentes é de 1:2. Portanto, ao se misturar volumes iguais, essa solução será neutra se a concentração de NaHCO3 for o dobro da concentração de H2SO4. Como a concentração do ácido sulfúrico é igual à concentração do bicarbonato de sódio, essa solução não é neutra.